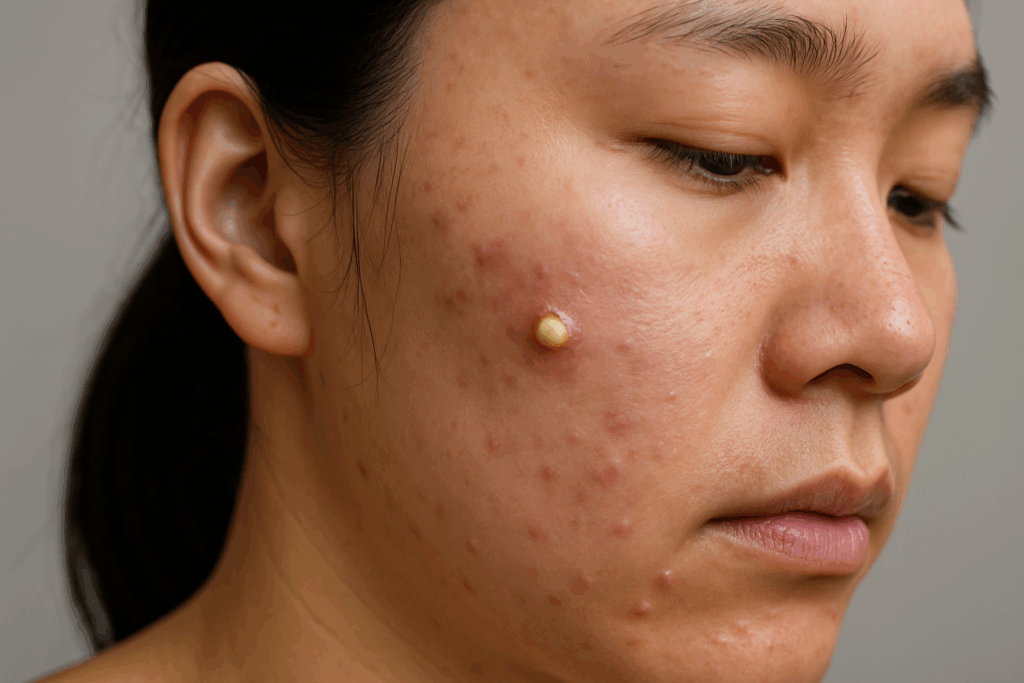
黄ニキビは、尋常性痤瘡の病態進行において最も重症化した段階を示す臨床像です。毛包内部で生じる炎症反応は、好中球の大量浸潤と組織破壊を伴いながら膿疱を形成し、皮膚表面に黄色調の隆起性病変として観察されます【文献1】。この膿疱性病変は、単なる皮脂貯留や細菌増殖だけでは説明できない、複雑な免疫学的カスケードと組織応答の結果として出現します【文献2】。しかし、なぜ毛包という微小な構造内で、これほど激しい炎症反応が惹起されるのでしょうか。そのメカニズムを理解するためには、分子レベルから組織レベルに至る多層的な病態生理学的プロセスを、段階的に解明する必要があります。
膿疱形成の本質は、毛包壁の構造的破綻と炎症性細胞の集積にあります。アクネ菌(Cutibacterium acnes)が産生する酵素群は、毛包上皮の基底膜を分解し、炎症性メディエーターを周囲組織へ放出させます【文献3】。この過程で、インターロイキン-1βやインターロイキン-8といった強力な炎症性サイトカインは、血管内皮細胞に作用して好中球の遊走を促進します【文献2】。集積した好中球は、活性酸素種とリソソーム酵素を放出し、毛包壁をさらに破壊します。このような連鎖反応により、初期の微小な炎症は、やがて肉眼的に確認できる膿疱性病変へと発展します【文献4】。したがって、黄ニキビの形成は、細菌感染に対する過剰な宿主応答として理解されます。
本稿では、黄ニキビの病態形成メカニズムを、臨床的定義から分子生物学的基盤まで、系統的に解説します。まず、膿疱性痤瘡としての臨床的特徴と組織学的所見を明確にし、次に、白ニキビから黄ニキビへと進行する段階的プロセスを記述します。その後、炎症カスケードの分子機構、Cutibacterium acnesの病原性因子、免疫細胞応答、そして毛包壁破裂による組織障害の拡大について、それぞれ詳述します。各項目では、実在する学術論文に基づく科学的根拠を提示し、膿疱がいかにして生じるのかという問いに対する、包括的な回答を構築します。
ニキビの種類と形成機序
- 白ニキビの病態と形成メカニズム—閉鎖面皰はいかにして生じるのか
- 黒ニキビの病態と形成メカニズム—開放面皰はいかにして生じるのか
- 赤ニキビの病態と形成メカニズム—紅色丘疹はいかにして生じるのか
- 黄ニキビの病態と形成メカニズム—膿疱はいかにして生じるのか
黄ニキビとは何か—膿疱性痤瘡の医学的定義と臨床的特徴
黄ニキビは、医学的には膿疱性痤瘡または膿疱性尋常性痤瘡と呼ばれ、尋常性痤瘡の炎症性病変のなかで最も重症度が高い臨床像を呈します【文献1】。この病変は、毛包脂腺系における炎症反応が極度に進行し、大量の膿が毛包内部に貯留した状態として定義されます。皮膚表面からは、直径5ミリメートル前後の黄白色調を呈する隆起性病変が観察され、触診では波動感を伴う柔らかい膨隆として認識されます。膿疱の中心部には、壊死した組織片、死滅した好中球、細菌の残骸、そして血清成分が混在しており、これらが黄色調の外観を形成します【文献3】。したがって、黄ニキビの「黄色」は、単なる色素沈着ではなく、炎症性滲出物の光学的特性に由来します。
組織学的観察では、黄ニキビの病変部において毛包壁の著しい破壊が確認されます。正常な毛包構造では、重層扁平上皮が毛包内腔を裏打ちし、その外側を基底膜が支持しています。しかし、膿疱性病変では、この基底膜が断裂し、毛包上皮細胞は壊死に陥ります【文献4】。破壊された毛包壁の周囲には、好中球を主体とする炎症性細胞が密集し、膿瘍様の構造を形成します。さらに、炎症は真皮層深部へと波及し、膠原線維の変性と毛細血管の拡張を伴います【文献9】。この組織学的所見は、黄ニキビが単なる表層的な炎症ではなく、皮膚の深部構造に及ぶ破壊的プロセスであることを示します。
臨床的には、黄ニキビは自発痛や圧痛を伴うことが多く、患者の日常生活の質を著しく低下させます。病変の周囲には発赤と腫脹が認められ、触診では熱感を伴います。これらの症状は、局所における炎症性メディエーターの高濃度集積と、血管透過性の亢進を反映しています【文献2】。また、黄ニキビは自然治癒後も、萎縮性瘢痕や色素沈着を残す傾向があります。これは、真皮層の膠原線維が不可逆的に破壊されたためであり、組織修復機構が完全には機能しないことを意味します【文献9】。したがって、黄ニキビの臨床的重要性は、急性期の症状だけでなく、長期的な美容上の問題にも及びます。
膿疱性病変の外観的特徴と鑑別診断上の留意点
黄ニキビの外観は、その病態進行度によって変化します。初期段階では、赤色丘疹の中心部にわずかな黄白色の点状領域が出現します。この段階では、膿の貯留量は少なく、毛包壁の破壊も限定的です。しかし、炎症が進行するにつれて、黄白色領域は拡大し、やがて病変全体を覆うようになります【文献3】。成熟した膿疱では、表皮が薄く伸展し、透過性が高まるため、内部の膿が明瞭に透見されます。この時期の病変は、軽微な外力によって容易に破裂し、膿性滲出液を排出します。破裂後の病変部には、びらんや浅い潰瘍が形成され、二次感染のリスクが高まります。
鑑別診断上、黄ニキビは他の膿疱性皮膚疾患と区別される必要があります。毛嚢炎は、黄ニキビと類似した外観を呈しますが、病変の分布と発生機序が異なります。毛嚢炎は主に黄色ブドウ球菌感染によって生じ、毛包の浅層部に限局した炎症を示します【文献1】。一方、黄ニキビは、アクネ菌の増殖と宿主免疫応答の相互作用によって発生し、毛包の深部から真皮層に及ぶ広範な炎症を伴います。また、膿疱性乾癬や好酸球性膿疱性毛嚢炎といった疾患も、膿疱を形成しますが、これらは全身性の炎症反応や特異的な免疫学的背景を有しており、尋常性痤瘡とは病態が根本的に異なります。したがって、正確な診断には、病変の分布、発症経過、組織学的所見を総合的に評価することが求められます。
黄ニキビに特異的な視診所見
黄ニキビの視診では、以下の特徴的所見が認められます。これらの所見は、膿疱性病変を他の炎症性皮膚疾患から鑑別する際の重要な手がかりとなります。
- 中心部の黄白色調の膿頭:病変の頂点に、直径2~5ミリメートルの黄白色領域が観察され、この部分には膿が高密度に集積しています。
- 周囲の紅斑と腫脹:膿疱を取り囲むように、直径10~20ミリメートルの発赤領域が広がり、炎症の範囲を示します。
- 表皮の菲薄化と光沢:膿の内圧によって表皮が伸展し、光を反射する滑らかな表面性状を呈します。
- 波動感の触知:指先で病変を軽く圧迫すると、液体貯留に特有の波動が感じられ、これは膿の存在を示唆します。
これらの視診所見は、黄ニキビの診断において高い特異性を持ちます。特に、中心部の黄白色調と周囲の紅斑の組み合わせは、膿疱性痤瘡に特徴的なパターンとして認識されます【文献3】。また、複数の病変が顔面、特に頬部や下顎部に集簇する傾向も、尋常性痤瘡の典型的な分布様式を反映しています【文献1】。ただし、これらの外観的特徴だけでは、病変内部の組織学的変化や分子レベルの炎症機序を完全には理解できません。したがって、黄ニキビの本質的な理解には、臨床所見に加えて、病態生理学的メカニズムの詳細な検討が不可欠です。
組織学的構造における特徴的変化
組織学的検査では、黄ニキビの病変部に以下の特徴的変化が確認されます。これらの変化は、膿疱形成の過程で生じる一連の組織破壊と炎症細胞浸潤を反映しています。
- 毛包壁の断裂と破壊:毛包上皮細胞の壊死と基底膜の断裂が広範に観察され、毛包の構造的完全性が失われています。
- 好中球の密集:破壊された毛包周囲には、好中球が高密度に集積し、膿瘍を形成しています。
- 真皮層への炎症波及:炎症は毛包を越えて真皮層深部に拡大し、膠原線維の変性と血管周囲への炎症細胞浸潤が認められます。
- 血管拡張と浮腫:真皮内の毛細血管は著しく拡張し、血管周囲には漿液性滲出液が貯留しています。
これらの組織学的所見は、黄ニキビが単なる毛包内の限局性炎症ではなく、周囲組織を巻き込む破壊的プロセスであることを明確に示します【文献4】。特に、毛包壁の断裂は、炎症性物質と細菌成分が真皮層へ流出する経路を形成し、炎症のさらなる拡大を招きます【文献3】。また、好中球の大量浸潤は、これらの細胞が放出するプロテアーゼと活性酸素種によって、組織破壊がさらに増幅されることを意味します【文献2】。このような組織学的変化の理解は、黄ニキビの形成メカニズムを解明する上で、基礎的な知見を提供します。
膿の構成成分と生化学的性状
黄ニキビの膿は、複数の生体成分が混合した複雑な組成を持ちます。主要な構成要素は、死滅した好中球とその断片化した核物質です。好中球は、炎症部位に遊走した後、貪食作用と活性酸素産生を行い、最終的にはアポトーシスまたは壊死によって死滅します【文献2】。死滅した好中球の核からは、DNAとヒストンが放出され、これらが膿の粘稠性を高めます。また、膿には大量のリソソーム酵素が含まれており、これらの酵素は周囲組織のタンパク質を分解し、炎症反応をさらに増幅させます【文献5】。さらに、血清由来のアルブミンやグロブリンも膿中に検出され、血管透過性の亢進を反映しています。
膿の生化学的分析では、高濃度の炎症性サイトカインが検出されます。特に、インターロイキン-1βとインターロイキン-8の濃度は、正常皮膚と比較して数十倍から数百倍に上昇しています【文献5】。インターロイキン-1βは、炎症反応の初期段階で産生され、他の炎症性メディエーターの発現を誘導します。インターロイキン-8は、強力な好中球走化因子として機能し、血管内から組織内への好中球遊走を促進します【文献2】。これらのサイトカインの高濃度集積は、膿疱内部が極めて強い炎症環境にあることを示します。また、膿中にはアクネ菌の細胞壁成分やリパーゼといった細菌由来物質も含まれており、これらが宿主免疫系を持続的に刺激します【文献3】。
膿のpHは、通常わずかに酸性を示し、これは好中球の代謝活動と組織破壊の結果として生じる乳酸の蓄積によります。酸性環境は、一部の細菌の増殖を抑制する一方で、タンパク質分解酵素の活性を高め、組織障害を増悪させる可能性があります。また、膿中の酸素分圧は低下しており、これは好中球の酸素消費と血流障害によって説明されます。低酸素環境は、アクネ菌のような嫌気性菌の増殖には有利ですが、組織修復機構には不利に作用します【文献3】。このように、膿疱内部の微小環境は、炎症の持続と組織破壊の進行を促進する複数の因子を含んでおり、これが黄ニキビの治療を困難にする一因となります。
膿中の主要細胞成分とその由来
黄ニキビの膿には、以下の細胞成分が高濃度に含まれています。これらの細胞は、炎症反応の過程で組織内に動員され、最終的には死滅して膿の一部を構成します。
- 好中球の残骸:膿の容積の大部分を占める成分であり、死滅した好中球の細胞膜断片、断片化したDNA、そして放出されたリソソーム酵素を含みます。
- 壊死したケラチノサイト:毛包上皮を構成していたケラチノサイトが、炎症反応によって壊死し、膿中に混入します。
- マクロファージ:炎症部位に遊走したマクロファージは、貪食作用を行った後、膿中に残存します。
- アクネ菌とその断片:生菌と死菌の両方が膿中に存在し、細胞壁成分や代謝産物も検出されます。
これらの細胞成分の分析は、黄ニキビの膿が単なる細菌感染の産物ではなく、複雑な宿主応答の結果であることを示します【文献2】。特に、好中球の大量動員と死滅は、膿疱形成の中心的なプロセスであり、これが黄色調の外観と粘稠な性状を生み出します。また、壊死したケラチノサイトの存在は、毛包上皮の広範な破壊を反映しており、組織修復の困難さを示唆します【文献4】。したがって、膿の構成成分の理解は、黄ニキビの病態メカニズムを解明する上で重要な情報を提供します。
炎症性メディエーターの濃度プロファイル
黄ニキビの膿中には、以下の炎症性メディエーターが高濃度に検出されます。これらのメディエーターは、炎症反応の増幅と持続に中心的な役割を果たします。
- インターロイキン-1α:ケラチノサイトから放出される初期炎症メディエーターであり、膿中濃度は正常皮膚の50倍以上に達します【文献5】。
- インターロイキン-1β:単球とマクロファージから産生され、好中球の活性化と血管透過性の亢進を誘導します【文献2】。
- インターロイキン-8:最も強力な好中球走化因子の一つであり、膿疱への好中球の持続的な動員を維持します【文献2】。
- 腫瘍壊死因子-α:炎症反応の全身化と組織破壊の増幅に関与し、血管内皮細胞の活性化を促進します。
これらの炎症性メディエーターの濃度プロファイルは、黄ニキビが極めて活発な炎症状態にあることを定量的に示します【文献5】。特に、インターロイキン-1βとインターロイキン-8の相乗効果は、好中球の持続的な動員と活性化を維持し、炎症反応の自己増幅サイクルを形成します【文献2】。また、これらのサイトカインは、毛包周囲の血管内皮細胞に接着分子の発現を誘導し、血管から組織への白血球の遊走を促進します。このような分子レベルでの炎症機序の理解は、黄ニキビの形成過程を包括的に説明する基盤となります。
黄ニキビが好発する解剖学的部位とその理由
黄ニキビは、顔面の特定の領域に好発する傾向があります。最も頻度が高いのは、頬部、下顎部、そして鼻周囲です【文献1】。これらの部位に共通する特徴は、脂腺が大型で密度が高く、皮脂分泌が旺盛であることです。顔面のTゾーンと呼ばれる額から鼻にかけての領域も、黄ニキビの好発部位として知られています。一方、眼瞼や口唇といった脂腺の少ない部位には、黄ニキビはほとんど発生しません。この分布パターンは、黄ニキビの発生が脂腺活動と密接に関連していることを示唆します【文献3】。また、思春期以降の男性では、胸部や背部上部にも黄ニキビが出現することがあり、これらの部位もまた脂腺密度が高い領域です。
顔面における黄ニキビの分布には、解剖学的要因が関与します。顔面皮膚の毛包は、他の部位と比較して大型で深い構造を持ち、これが炎症の拡大を容易にします。特に、頬部の毛包は真皮深層まで達しており、炎症が深部組織に波及しやすい構造的特徴を有します【文献4】。また、顔面皮膚は表情筋の運動や咀嚼運動によって常に機械的ストレスを受けており、これが毛包壁の微小損傷を引き起こし、炎症の起点となる可能性があります。さらに、顔面は外部環境との接触が多く、化粧品、汗、皮脂、そして大気中の汚染物質といった様々な刺激因子に曝露されます。これらの因子は、毛包内環境を変化させ、炎症反応を誘発または増悪させる可能性があります【文献1】。
内分泌学的要因も、黄ニキビの好発部位に影響を与えます。顔面と胸背部の脂腺は、アンドロゲン受容体を高密度に発現しており、性ホルモンの影響を強く受けます。思春期や月経周期に伴うアンドロゲンレベルの変動は、これらの部位の皮脂分泌を増加させ、毛包内環境を変化させます【文献1】。また、ストレスによるコルチゾール分泌の亢進も、脂腺活動を刺激し、黄ニキビの発生リスクを高めます。このように、黄ニキビの好発部位は、解剖学的構造、機械的ストレス、外部環境因子、そして内分泌学的影響が複合的に作用する結果として決定されます。したがって、黄ニキビの臨床的特徴を理解するには、これらの多様な要因を統合的に考慮する必要があります。
顔面における好発部位の解剖学的特性
黄ニキビが好発する顔面の各部位は、以下の解剖学的特性を共有しています。これらの特性は、膿疱形成のリスクを高める構造的基盤を提供します。
- 脂腺の大型化と高密度分布:頬部と鼻周囲には、直径1~2ミリメートルの大型脂腺が密集しており、単位面積あたりの皮脂分泌量が他の部位よりも多くなります。
- 毛包の深在性:これらの部位の毛包は真皮深層まで達しており、炎症が深部組織に波及しやすい構造を持ちます。
- 豊富な血管網:顔面皮膚は毛細血管が密に分布しており、炎症性細胞の供給と炎症性メディエーターの拡散が効率的に行われます。
- 表情筋による機械的刺激:頬部や下顎部の皮膚は表情筋の収縮によって常に動的な力を受け、これが毛包壁に微小な損傷を与える可能性があります。
これらの解剖学的特性の組み合わせは、黄ニキビの発生に有利な条件を作り出します【文献3】。特に、脂腺の大型化は皮脂の過剰産生を招き、これがアクネ菌の増殖基質となります。また、毛包の深在性は、一度炎症が発生すると、それが容易に真皮層深部へ拡大することを意味します【文献4】。したがって、黄ニキビの好発部位を理解することは、その病態形成メカニズムを解明する上で重要な手がかりとなります。
ニキビ進行の段階的プロセス—白ニキビから黄ニキビへの病態移行
尋常性痤瘡の病態は、微小面皰から膿疱性病変に至るまで、明確な段階的進行を示します。この進行過程は、毛包内環境の変化、細菌増殖、そして免疫応答の段階的活性化という、相互に関連する三つの要素によって駆動されます【文献3】。初期段階では、毛包漏斗部における角化異常が生じ、皮脂と角質が毛包内に貯留します。この状態が微小面皰であり、肉眼的には観察できない前臨床段階です【文献4】。微小面皰は、すべての痤瘡病変の起点となる基本的構造であり、この段階で適切な介入が行われなければ、病態はさらに進行します。微小面皰内部では、酸素分圧が低下し、嫌気性環境が形成されることで、アクネ菌の増殖に有利な条件が整います。
微小面皰から白ニキビへの移行は、毛包内圧の上昇と毛包開口部の閉塞によって特徴づけられます。白ニキビは、閉鎖面皰とも呼ばれ、毛包開口部が完全に閉塞した状態を示します【文献1】。この段階では、皮脂と角質の蓄積がさらに進行し、毛包は球状に拡張します。毛包内部ではアクネ菌が急速に増殖し、その数は正常皮膚と比較して数百倍に達します【文献3】。しかし、この段階では炎症反応はまだ顕著ではなく、組織学的にも炎症細胞の浸潤は軽度です。白ニキビの外観は、皮膚表面にわずかに隆起した白色の丘疹として観察され、触診では硬い感触を呈します。この硬さは、高密度に充填された皮脂と角質によるものです。
白ニキビから赤ニキビへの進行は、炎症反応の本格的な開始を意味します。この段階では、アクネ菌が産生するリパーゼが皮脂中のトリグリセリドを分解し、遊離脂肪酸を生成します【文献3】。遊離脂肪酸は、毛包上皮を刺激し、炎症性サイトカインの産生を誘導します。特に、インターロイキン-1αは、この段階で大量に放出され、炎症反応の初期シグナルとして機能します【文献5】。また、アクネ菌の細胞壁成分は、毛包周囲の免疫細胞によって認識され、Toll様受容体2を介したシグナル伝達が活性化されます【文献2】。この免疫応答により、炎症性サイトカインとケモカインの産生がさらに増幅され、好中球とマクロファージの遊走が開始されます。赤ニキビは、臨床的には発赤を伴う圧痛のある丘疹として観察され、組織学的には毛包周囲への炎症細胞浸潤が確認されます【文献4】。
微小面皰形成の分子機構と初期変化
微小面皰の形成は、毛包漏斗部のケラチノサイトにおける異常な角化プロセスから始まります。正常な毛包では、ケラチノサイトは規則的に分化し、最終的には角質細胞として剥離します。しかし、痤瘡の初期段階では、ケラチノサイトの増殖速度が亢進し、同時に細胞間接着が強化されます【文献4】。この結果、角質細胞は毛包内腔に蓄積し、毛包開口部を部分的に閉塞します。この過程には、複数の分子機構が関与しています。まず、アンドロゲンが毛包ケラチノサイトのアンドロゲン受容体に結合し、細胞増殖関連遺伝子の発現を誘導します【文献1】。また、インターロイキン-1αのような炎症性サイトカインも、ケラチノサイト増殖を刺激する作用を持ちます【文献5】。
微小面皰内部では、皮脂の組成変化も重要な役割を果たします。正常な皮脂は、トリグリセリド、ワックスエステル、スクワレン、そして少量の遊離脂肪酸で構成されます。しかし、微小面皰では、スクワレンの酸化が進行し、過酸化スクワレンが生成されます【文献10】。過酸化スクワレンは、ケラチノサイトに対して直接的な刺激作用を持ち、炎症性メディエーターの産生を誘導します。また、過酸化脂質は毛包上皮のバリア機能を低下させ、外来抗原の侵入を容易にします。このような脂質環境の変化は、微小面皰から炎症性病変への進行を促進する重要な因子となります【文献10】。さらに、微小面皰内部の酸素分圧は正常毛包と比較して著しく低下しており、これがアクネ菌の増殖に最適な環境を提供します【文献3】。
微小面皰の形成初期段階では、組織学的にも特徴的な変化が観察されます。毛包漏斗部の上皮は肥厚し、細胞層の数が増加します。基底層のケラチノサイトは活発に分裂しており、有糸分裂像が頻繁に認められます【文献4】。また、顆粒層の細胞ではケラトヒアリン顆粒の形成が不完全であり、角化過程の異常を示唆します。毛包内腔には、不完全に角化した細胞と皮脂が混在して蓄積し、これが微小面皰の内容物を構成します。この段階では、炎症細胞の浸潤はごくわずかであり、主に散在性のリンパ球が毛包周囲に認められる程度です【文献3】。しかし、免疫組織化学的検査では、毛包上皮におけるインターロイキン-1αの発現が既に上昇しており、炎症反応の準備段階にあることが示されます【文献5】。
毛包漏斗部における角化異常の開始因子
微小面皰形成の引き金となる角化異常は、以下の因子によって開始されます。これらの因子は、単独または複合的に作用し、毛包内環境を変化させます。
- アンドロゲン刺激の増強:テストステロンとジヒドロテストステロンが毛包ケラチノサイトのアンドロゲン受容体に結合し、細胞増殖と皮脂分泌を促進します【文献1】。
- インターロイキン-1αの基底レベル上昇:ケラチノサイトが産生するインターロイキン-1αは、細胞増殖を刺激し、角化過程を変調させます【文献5】。
- 皮脂組成の変化:スクワレンの過酸化や遊離脂肪酸の増加が、毛包上皮に刺激を与え、角化異常を誘発します【文献10】。
- レチノイン酸シグナルの減弱:ビタミンA誘導体であるレチノイン酸の局所濃度低下は、正常な角化プロセスの維持を困難にします。
これらの因子の相互作用により、毛包漏斗部のケラチノサイトは異常な増殖パターンを示すようになります【文献4】。特に、アンドロゲン刺激とインターロイキン-1αの相乗効果は、ケラチノサイトの増殖速度を著しく加速させます【文献1】【文献5】。また、皮脂組成の変化は、毛包内の物理化学的環境を変化させ、正常な角質剥離プロセスを阻害します【文献10】。このように、微小面皰形成は、内分泌因子、炎症性メディエーター、そして脂質代謝異常が統合された結果として生じます。
微小面皰内部の微小環境特性
微小面皰の内部では、以下のような特徴的な微小環境が形成されます。この環境は、アクネ菌の増殖と炎症反応の準備を促進します。
- 酸素分圧の低下:毛包開口部の部分閉塞により、酸素供給が制限され、嫌気性環境が形成されます。酸素分圧は正常毛包の10分の1以下に低下します【文献3】。
- pH値の微酸性化:皮脂と角質の代謝により、微小面皰内のpHはわずかに酸性側に傾きます。この環境はアクネ菌の至適増殖条件に適合します。
- 栄養基質の集積:皮脂中のトリグリセリドと角質タンパク質が高濃度に蓄積し、アクネ菌の増殖に必要な栄養源を提供します【文献3】。
- 抗菌ペプチドの相対的減少:正常皮膚では抗菌ペプチドが皮膚表面を保護していますが、閉塞された微小面皰内部ではこれらの防御因子の濃度が低下します。
これらの微小環境特性は、微小面皰からより進行した病変への移行を促進する基盤となります【文献3】。特に、酸素分圧の低下は、偏性嫌気性菌であるアクネ菌に選択的な増殖優位性を与えます。また、栄養基質の集積は、細菌の指数関数的増殖を可能にします【文献3】。さらに、抗菌ペプチドの減少は、宿主の自然免疫防御機構が十分に機能しないことを意味し、細菌増殖の制御が困難になります。このような微小環境の理解は、痤瘡病態の初期段階における介入ポイントを特定する上で重要です。
白ニキビから赤ニキビへの移行と炎症開始
白ニキビから赤ニキビへの移行は、痤瘡病態において最も重要な転換点です。この段階で、非炎症性病変から炎症性病変への質的変化が生じます【文献3】。移行の契機となるのは、アクネ菌が産生する複数の病原性因子です。まず、アクネ菌のリパーゼは、毛包内に貯留した皮脂のトリグリセリドを加水分解し、遊離脂肪酸を生成します【文献3】。遊離脂肪酸、特に飽和脂肪酸は、毛包上皮に対して強い刺激作用を持ち、ケラチノサイトからの炎症性サイトカイン放出を誘導します。この段階で、インターロイキン-1α、インターロイキン-8、そして腫瘍壊死因子-αといった主要な炎症性メディエーターの産生が急激に増加します【文献5】。
アクネ菌の細胞壁成分、特にペプチドグリカンとリポテイコ酸は、パターン認識受容体を介して宿主免疫系に認識されます【文献2】。毛包周囲のケラチノサイトとマクロファージは、Toll様受容体2を発現しており、これがアクネ菌成分を感知します。Toll様受容体2の活性化は、核内因子κB(NF-κB)シグナル伝達経路を活性化し、炎症性遺伝子の転写を促進します【文献2】。この結果、インターロイキン-1β、インターロイキン-6、インターロイキン-8といった多様なサイトカインとケモカインが産生されます。これらのメディエーターは、血管内皮細胞に作用し、接着分子の発現を誘導します。血管内皮細胞上に発現したE-セレクチンとICAM-1は、血流中の好中球とリンパ球を捕捉し、組織内への遊走を開始させます【文献4】。
赤ニキビの組織学的特徴は、毛包周囲への炎症細胞浸潤です。初期段階では、主にリンパ球とマクロファージが毛包周囲の真皮に集積します【文献3】。これらの細胞は、アクネ菌抗原を認識し、さらなる炎症性メディエーターを放出します。特に、マクロファージから産生される腫瘍壊死因子-αとインターロイキン-1βは、炎症反応を増幅する中心的な役割を果たします【文献2】。炎症が進行するにつれて、好中球の浸潤も開始されます。好中球は、インターロイキン-8に誘導されて毛包周囲に遊走し、活性酸素種とプロテアーゼを放出します【文献2】。この段階では、毛包壁の構造的完全性はまだ維持されていますが、上皮細胞の一部には変性と壊死の兆候が認められます【文献4】。臨床的には、赤ニキビは発赤、腫脹、そして圧痛を伴う丘疹として観察され、患者は明確な不快感を自覚します。
炎症開始に関与する主要な分子シグナル
白ニキビから赤ニキビへの移行時に活性化される主要な分子シグナルは、以下の通りです。これらのシグナルは、炎症反応の開始と増幅を制御します。
- Toll様受容体2シグナル:アクネ菌の細胞壁成分がToll様受容体2に結合し、MyD88を介したシグナル伝達が活性化され、NF-κBが核内に移行して炎症性遺伝子の転写を促進します【文献2】。
- NF-κB経路の活性化:核内因子κBは、インターロイキン-1β、インターロイキン-6、インターロイキン-8、腫瘍壊死因子-αといった多数の炎症性サイトカイン遺伝子のプロモーター領域に結合し、転写を開始します。
- MAPKカスケードの活性化:マイトジェン活性化プロテインキナーゼ経路が活性化され、AP-1転写因子を介して炎症性遺伝子発現がさらに増強されます。
- 補体系の活性化:アクネ菌の細胞壁多糖体が補体の副経路を活性化し、C5aなどの走化性因子が生成され、好中球の動員が促進されます【文献3】。
これらの分子シグナルの同時活性化は、炎症反応を急速に増幅させます【文献2】。特に、Toll様受容体2シグナルとNF-κB経路の活性化は、炎症性サイトカインの産生において中心的な役割を果たします【文献2】。また、MAPK経路は、サイトカイン産生に加えて、マトリックスメタロプロテアーゼの発現も誘導し、組織リモデリングと破壊に寄与します。補体系の活性化は、好中球の迅速な動員を可能にし、炎症反応を組織レベルに拡大させます【文献3】。このような多層的な分子機構の理解は、赤ニキビから黄ニキビへのさらなる進行を説明する基盤となります。
赤ニキビにおける免疫細胞の初期応答
赤ニキビの段階では、以下の免疫細胞が順次動員され、炎症反応を担います。これらの細胞の相互作用が、病態のさらなる進行を決定します。
- マクロファージの早期浸潤:組織常在性マクロファージがアクネ菌成分を認識し、炎症性サイトカインの産生を開始します。この段階のマクロファージは、M1型の炎症促進性表現型を示します【文献3】。
- 樹状細胞による抗原提示:毛包周囲の樹状細胞がアクネ菌抗原を取り込み、所属リンパ節へ移動して抗原特異的T細胞を活性化します。
- CD4陽性T細胞の動員:活性化されたヘルパーT細胞が炎症部位に遊走し、インターフェロン-γやインターロイキン-17といったサイトカインを産生します【文献2】。
- 好中球の初期浸潤:インターロイキン-8に応答して好中球が血管から組織内に遊走し始めますが、この段階ではまだ数は限定的です【文献2】。
これらの免疫細胞の段階的動員は、赤ニキビから黄ニキビへの進行過程を準備します【文献3】。マクロファージとT細胞の活性化は、炎症反応を慢性化させ、持続的なサイトカイン産生を維持します【文献2】。特に、インターロイキン-17を産生するTh17細胞の関与は、好中球の大量動員を促進し、膿疱形成への道を開きます【文献2】。この段階での免疫応答の強度と持続期間が、最終的に黄ニキビへと進行するか、あるいは赤ニキビの段階で炎症が収束するかを決定する重要な因子となります【文献4】。
赤ニキビから黄ニキビへの進行と膿疱化の開始
赤ニキビから黄ニキビへの進行は、好中球の大量浸潤と毛包壁の破綻によって特徴づけられます。この段階では、炎症反応がさらに激化し、組織破壊が本格的に開始されます【文献4】。赤ニキビの段階で産生されたインターロイキン-8は、骨髄から好中球を動員し、血管内皮を通過させて炎症部位へ誘導します【文献2】。好中球は、炎症部位に到達すると、まずアクネ菌の貪食を試みます。しかし、毛包内部のアクネ菌は、バイオフィルムを形成している場合があり、好中球の貪食作用から部分的に保護されています【文献3】。また、アクネ菌の一部は、ケラチノサイトや脂腺細胞の内部に侵入しており、これも好中球による除去を困難にします。
貪食作用が不完全である場合、好中球は細胞外に活性酸素種とプロテアーゼを放出します【文献2】。活性酸素種、特にスーパーオキシドアニオンと過酸化水素は、周囲組織に対して無差別な酸化障害を与えます。また、好中球エラスターゼ、カテプシン、そしてマトリックスメタロプロテアーゼといったプロテアーゼは、毛包壁を構成する膠原線維とエラスチン線維を分解します【文献4】。この酵素的分解により、毛包壁は次第に薄くなり、機械的強度を失います。さらに、アクネ菌自身が産生するリパーゼとプロテアーゼも、毛包壁の破壊に寄与します【文献3】。アクネ菌リパーゼは、毛包上皮細胞の細胞膜脂質を分解し、細胞の完全性を損ないます。このような多方向からの攻撃により、毛包壁は最終的に破綻します。
毛包壁が破綻すると、毛包内容物が真皮層へ流出します【文献4】。流出する物質には、アクネ菌とその代謝産物、皮脂、角質、そして既に集積していた炎症性細胞が含まれます。これらの物質は、真皮層の免疫細胞に対して強力な刺激となります。特に、アクネ菌の細胞壁成分は、真皮内のマクロファージとマスト細胞を活性化し、さらなる炎症性メディエーターの放出を誘導します【文献3】。この段階で、炎症は毛包の境界を越えて周囲組織に拡大し、より広範な組織破壊が生じます【文献4】。好中球の浸潤はさらに加速され、毛包周囲に大量の好中球が集積します。これらの好中球の多くは、やがて死滅してアポトーシスまたは壊死に至り、その残骸が膿の主要成分となります【文献2】。臨床的には、この段階で病変は明らかな膿疱性外観を呈するようになり、黄ニキビとして認識されます。
好中球大量動員を誘導するケモカインカスケード
赤ニキビから黄ニキビへの移行期には、以下のケモカインが協調的に作用し、好中球の大量動員を実現します。これらのケモカインの濃度勾配が、好中球の効率的な遊走を可能にします。
- インターロイキン-8(CXCL8):最も強力な好中球走化因子であり、ケラチノサイトとマクロファージから大量に産生されます。インターロイキン-8は、好中球表面のCXCR1とCXCR2受容体に結合し、細胞の遊走と活性化を誘導します【文献2】。
- GRO-α(CXCL1):インターロイキン-8と同様にCXCR2に結合し、好中球の動員を補完します。GRO-αは、血管内皮細胞からも産生され、好中球の血管外遊出を促進します。
- 補体C5a:補体系の活性化によって生成され、強力な好中球走化作用を持ちます。C5aは、好中球の活性酸素産生能力も増強します【文献3】。
- ロイコトリエンB4:アラキドン酸代謝経路から生成される脂質メディエーターであり、好中球の遊走と活性化を促進します。ロイコトリエンB4は、炎症部位の血管透過性も亢進させます。
これらのケモカインとメディエーターの協調作用により、毛包周囲への好中球の集積は指数関数的に増加します【文献2】。特に、インターロイキン-8とC5aの相乗効果は、好中球動員において極めて重要です【文献2】【文献3】。また、これらのメディエーターは、好中球の活性化状態も制御し、活性酸素産生やプロテアーゼ放出を増強します【文献2】。このような多層的な好中球動員機構の理解は、黄ニキビにおける膿疱形成の本質を説明する鍵となります。
毛包壁破綻の組織学的段階
赤ニキビから黄ニキビへの移行過程における毛包壁の破綻は、以下の段階を経て進行します。各段階は、特定の組織学的変化によって特徴づけられます。
- 上皮細胞の変性開始:毛包上皮細胞が、炎症性メディエーターと活性酸素による障害を受け、細胞質の空胞化と核の濃縮が観察されます。この段階では、まだ基底膜の連続性は保たれています【文献4】。
- 基底膜の部分的断裂:プロテアーゼによる分解が進行し、基底膜に微小な断裂が生じます。この断裂部位から、炎症性細胞が毛包内腔に侵入し始めます【文献4】。
- 上皮層の広範な壊死:炎症がさらに激化すると、毛包上皮細胞は大規模に壊死に陥ります。壊死した細胞は、毛包内腔と真皮層の間の障壁としての機能を喪失します【文献4】。
- 毛包内容物の真皮流出:毛包壁の完全な破綻により、内容物が周囲の真皮層へ流出し、炎症は毛包の境界を越えて拡大します。この段階で、膿疱性病変が確立します【文献4】。
この段階的破綻プロセスは、組織学的観察によって明確に確認されます【文献4】。各段階は可逆的ではなく、一度進行が始まると、組織修復機構が介入しない限り、最終的な毛包壁破綻へと至ります。特に、基底膜の断裂は、病態進行における重要な転換点であり、この段階を過ぎると炎症の制御は著しく困難になります【文献4】。
黄ニキビ形成の分子生物学的メカニズム—炎症カスケードと膿疱化の過程
黄ニキビの形成は、複数の炎症性シグナル伝達経路が統合的に活性化された結果として生じます。この過程の中心に位置するのは、インフラマソームと呼ばれる多タンパク質複合体の活性化です【文献6】。インフラマソームは、細胞質内でパターン認識受容体、アダプタータンパク質、そしてプロカスパーゼ-1が会合して形成される構造体であり、炎症性サイトカインの成熟と放出を制御します【文献2】。アクネ菌の感染は、NLRP3インフラマソームを活性化し、プロカスパーゼ-1を活性型カスパーゼ-1へと変換します【文献6】。活性化されたカスパーゼ-1は、プロインターロイキン-1βとプロインターロイキン-18を切断し、成熟した活性型サイトカインを産生します【文献2】。成熟インターロイキン-1βは、細胞外に放出され、周囲の細胞に作用して炎症反応を増幅します。
インターロイキン-1βは、黄ニキビ形成における最も重要な炎症性メディエーターの一つです【文献2】。このサイトカインは、ケラチノサイト、マクロファージ、そして脂腺細胞の表面に発現するインターロイキン-1受容体に結合し、細胞内シグナル伝達を開始します【文献7】。受容体への結合は、MyD88アダプタータンパク質を介したシグナルカスケードを活性化し、最終的にはNF-κBとMAPKの両経路を同時に活性化します【文献2】。この結果、インターロイキン-6、インターロイキン-8、腫瘍壊死因子-α、そしてシクロオキシゲナーゼ-2といった多数の炎症関連遺伝子の転写が促進されます【文献2】。特に、インターロイキン-8の産生増加は、好中球の持続的な動員を維持し、膿疱内への好中球集積を加速させます【文献2】。また、インターロイキン-1βは、血管内皮細胞に接着分子の発現を誘導し、白血球の血管外遊出を促進します【文献2】。
脂腺細胞におけるインフラマソーム活性化も、黄ニキビ形成に重要な役割を果たします【文献7】。脂腺細胞は、単なる脂質産生細胞ではなく、免疫応答にも積極的に関与する細胞です。アクネ菌刺激を受けた脂腺細胞は、NLRP3インフラマソームを活性化し、インターロイキン-1βを産生します【文献7】。脂腺細胞由来のインターロイキン-1βは、脂腺自身の脂質代謝を変化させるとともに、周囲のケラチノサイトと免疫細胞を活性化します【文献7】。さらに、脂腺細胞はインターロイキン-6とインターロイキン-8も産生し、炎症反応の局所増幅に寄与します【文献7】。このように、脂腺細胞は、脂質産生と免疫応答の両機能を担う、痤瘡病態の中心的プレーヤーとして機能します【文献7】。脂腺細胞における炎症性シグナルの持続的活性化は、毛包脂腺系全体の炎症環境を維持し、膿疱形成を促進します【文献7】。
NLRP3インフラマソーム活性化の分子機構
NLRP3インフラマソームの活性化は、二段階のシグナルによって制御されます【文献6】。第一段階は、プライミングシグナルと呼ばれ、Toll様受容体やサイトカイン受容体を介してNF-κB経路が活性化されます【文献2】。このプライミングシグナルにより、NLRP3タンパク質とプロインターロイキン-1βの発現量が増加します【文献6】。アクネ菌の細胞壁成分は、Toll様受容体2を刺激してこのプライミングを誘導します【文献2】。第二段階は、活性化シグナルと呼ばれ、細胞内での特定の変化がNLRP3の立体構造変化とインフラマソーム複合体の形成を誘導します【文献6】。アクネ菌感染細胞では、カリウムイオンの細胞外流出、活性酸素種の産生、そしてリソソーム膜の破綻といった複数の活性化シグナルが生じます【文献6】。
カリウムイオン流出は、NLRP3活性化における最も重要なトリガーの一つです【文献6】。正常な細胞では、細胞内カリウム濃度は細胞外よりも高く維持されています。しかし、アクネ菌が産生する孔形成毒素や、炎症反応によって発現するP2X7受容体の活性化は、細胞膜にカリウムイオンの流出経路を形成します【文献6】。細胞内カリウム濃度の低下は、NLRP3タンパク質の構造変化を誘導し、ASCアダプタータンパク質との結合を促進します【文献6】。ASCは、NLRP3とプロカスパーゼ-1を架橋し、カスパーゼ-1の自己切断と活性化を可能にします【文献6】。活性化されたカスパーゼ-1は、プロインターロイキン-1βのN末端ドメインを切断し、成熟した17キロダルトンのインターロイキン-1βを生成します【文献2】。
活性酸素種の産生も、NLRP3インフラマソーム活性化に寄与します【文献6】。アクネ菌感染細胞では、ミトコンドリアと好中球由来のNADPHオキシダーゼの両方から活性酸素種が産生されます【文献6】。活性酸素種は、細胞内の酸化還元バランスを変化させ、NLRP3の酸化修飾を誘導します【文献6】。酸化修飾されたNLRP3は、より容易にインフラマソーム複合体を形成します【文献6】。さらに、活性酸素種はリソソーム膜を障害し、カテプシンBなどのリソソーム内プロテアーゼを細胞質に放出させます【文献6】。細胞質に放出されたカテプシンBは、NLRP3インフラマソームの活性化を促進する追加シグナルとして機能します【文献6】。このように、複数の細胞内変化が協調的に作用し、NLRP3インフラマソームの強力な活性化を実現します【文献6】。
インフラマソーム活性化の二段階制御機構
NLRP3インフラマソームの活性化は、以下の二段階で厳密に制御されます。この二段階機構により、過剰な炎症反応が抑制される一方で、必要時には迅速な応答が可能となります。
- 第一シグナル(プライミング):Toll様受容体2がアクネ菌の細胞壁成分を認識し、NF-κB経路を活性化します。これにより、NLRP3遺伝子とIL1B遺伝子の転写が促進され、タンパク質発現量が増加します【文献2】【文献6】。
- 第二シグナル(活性化):細胞内カリウム濃度の低下、活性酸素種の産生、リソソーム膜の破綻といった複数の細胞内変化が生じ、NLRP3タンパク質の構造変化とインフラマソーム複合体の形成を誘導します【文献6】。
- 複合体形成:NLRP3、ASC、プロカスパーゼ-1が会合し、大型の多量体複合体を形成します。この複合体内でプロカスパーゼ-1の自己切断が生じ、活性型カスパーゼ-1が生成されます【文献6】。
- 基質切断:活性化されたカスパーゼ-1が、プロインターロイキン-1βとプロインターロイキン-18を切断し、成熟型サイトカインへと変換します【文献2】【文献6】。
この二段階制御機構は、インフラマソーム活性化の特異性と強度を調節します【文献6】。第一シグナルのみでは、成熟インターロイキン-1βは産生されず、第二シグナルが加わって初めて活性化が完了します【文献6】。黄ニキビの病変部では、アクネ菌感染と組織損傷の両方が存在するため、第一と第二のシグナルが同時に供給され、強力なインフラマソーム活性化が持続します【文献2】【文献6】。この持続的活性化が、大量のインターロイキン-1β産生と、それに伴う激しい炎症反応を引き起こします【文献2】。
カスパーゼ-1による基質タンパク質の切断反応
活性化されたカスパーゼ-1は、以下の基質タンパク質を特異的に認識し、切断します。これらの切断反応が、炎症性サイトカインの成熟と放出を制御します。
- プロインターロイキン-1β切断:31キロダルトンの前駆体タンパク質が、Asp116残基のC末端側で切断され、17キロダルトンの成熟型インターロイキン-1βが生成されます【文献2】。
- プロインターロイキン-18切断:24キロダルトンの前駆体が切断され、18キロダルトンの成熟型インターロイキン-18が産生されます。インターロイキン-18は、Th1型免疫応答を促進し、インターフェロン-γ産生を誘導します【文献6】。
- ガスダーミンD切断:ガスダーミンDは、カスパーゼ-1によって切断されると、細胞膜に孔を形成し、細胞のパイロトーシス(炎症性細胞死)を誘導します。この過程で、細胞内のインターロイキン-1βが細胞外へ放出されます【文献6】。
- その他の基質:カスパーゼ-1は、複数の代謝酵素や細胞骨格タンパク質も切断し、細胞機能に広範な影響を与えます【文献6】。
これらの切断反応は、炎症反応の増幅に直接的に寄与します【文献2】【文献6】。特に、インターロイキン-1βの成熟と放出は、周囲細胞への炎症シグナル伝達を開始し、炎症の空間的拡大を促進します【文献2】。また、パイロトーシスによる細胞死は、細胞内容物を細胞外へ放出し、さらなる炎症刺激となります【文献6】。黄ニキビの病変部では、これらの反応が同時多発的に生じており、炎症の自己増幅サイクルが形成されます【文献2】【文献6】。
炎症性サイトカインネットワークと相乗効果
黄ニキビの病変部では、複数の炎症性サイトカインが協調的に作用し、炎症反応を増幅します【文献2】。インターロイキン-1βとインターロイキン-8の相互作用は、この炎症性ネットワークの中核を成します【文献2】。インターロイキン-1βは、ケラチノサイトとマクロファージに作用し、インターロイキン-8の産生を誘導します【文献2】。産生されたインターロイキン-8は、血管内皮細胞と好中球に作用し、好中球の組織内遊走を促進します【文献2】。遊走してきた好中球は、活性酸素種とプロテアーゼを放出し、組織障害を引き起こします。この組織障害は、さらなるインフラマソーム活性化とインターロイキン-1β産生を誘導し、正のフィードバックループを形成します【文献2】。
腫瘍壊死因子-αもまた、重要な炎症性メディエーターです【文献8】。このサイトカインは、主にマクロファージから産生され、血管内皮細胞に作用して接着分子の発現を誘導します【文献8】。E-セレクチン、ICAM-1、VCAM-1といった接着分子の発現増加は、白血球の血管壁への接着と血管外遊出を促進します【文献8】。また、腫瘍壊死因子-αは、ケラチノサイトに作用してインターロイキン-6とインターロイキン-8の産生を増強します【文献8】。さらに、腫瘍壊死因子-αは、好中球の活性化状態を維持し、活性酸素産生能力を高めます【文献8】。このように、腫瘍壊死因子-αは、炎症細胞の動員、活性化、そして組織障害の全過程に関与します【文献8】。
インターロイキン-6は、炎症反応の慢性化に寄与します【文献2】。このサイトカインは、局所で産生されるだけでなく、全身循環にも入り、肝臓での急性期タンパク質産生を刺激します。局所では、インターロイキン-6はT細胞の分化と増殖を促進し、Th17細胞の分化を誘導します【文献2】。Th17細胞は、インターロイキン-17を産生し、好中球の動員をさらに増強します【文献2】。また、インターロイキン-6は、ケラチノサイトの増殖を刺激し、表皮肥厚を引き起こします。このような多様な作用により、インターロイキン-6は炎症反応の持続と拡大に寄与します【文献2】。黄ニキビの病変部では、これらのサイトカインが同時に高濃度で存在し、複雑な相互作用ネットワークを形成しています【文献2】。この炎症性サイトカインネットワークの理解は、黄ニキビにおける激しい炎症反応のメカニズムを説明する鍵となります【文献2】。
主要炎症性サイトカインの産生細胞と標的細胞
黄ニキビの病変部における主要な炎症性サイトカインは、以下の細胞から産生され、特定の標的細胞に作用します。これらの相互作用が、炎症ネットワークを構築します。
- インターロイキン-1β:ケラチノサイト、マクロファージ、脂腺細胞から産生され、これらの細胞自身に加えて、血管内皮細胞、線維芽細胞、T細胞に作用します【文献2】【文献7】。
- インターロイキン-8:ケラチノサイト、マクロファージ、脂腺細胞、血管内皮細胞から産生され、主に好中球に作用して走化性と活性化を誘導します【文献2】【文献7】。
- 腫瘍壊死因子-α:マクロファージとTh1細胞から産生され、血管内皮細胞、ケラチノサイト、線維芽細胞に作用し、接着分子発現と炎症性メディエーター産生を促進します【文献8】。
- インターロイキン-6:マクロファージ、ケラチノサイト、線維芽細胞から産生され、T細胞、B細胞、肝細胞に作用し、免疫応答の調節と急性期反応を誘導します【文献2】。
これらのサイトカインの産生細胞と標的細胞の関係は、炎症反応の空間的・時間的パターンを決定します【文献2】。特に、ケラチノサイトとマクロファージが複数のサイトカインを産生することで、これらの細胞が炎症反応の中心的な調節者として機能します【文献2】。また、産生されたサイトカインが産生細胞自身にもフィードバック作用を及ぼすことで、炎症の自己増幅が生じます【文献2】。このような複雑な細胞間相互作用の理解は、黄ニキビにおける持続的炎症のメカニズムを解明する基盤となります【文献2】。
サイトカイン間の相乗的相互作用
黄ニキビの病変部では、以下のサイトカイン間相互作用が相乗効果を生み出し、炎症反応を増幅します。これらの相互作用は、単独のサイトカイン作用よりも強力な生物学的効果を示します。
- インターロイキン-1βと腫瘍壊死因子-αの相乗効果:両サイトカインが同時に作用すると、ケラチノサイトからのインターロイキン-8産生が相乗的に増加し、好中球動員が著しく促進されます【文献2】。
- インターロイキン-1βとインターロイキン-6の協調作用:インターロイキン-1βがTh17細胞への分化を開始し、インターロイキン-6がその分化を完成させます。この結果、インターロイキン-17産生が増加し、好中球動員がさらに強化されます【文献2】。
- インターロイキン-8と補体C5aの共同効果:両走化因子が同時に存在すると、好中球の遊走速度が加速され、炎症部位への集積効率が向上します【文献2】。
- 腫瘍壊死因子-αとインターフェロン-γの相互増強:両サイトカインは、マクロファージのM1型活性化を相乗的に促進し、炎症性メディエーター産生と活性酸素産生を増強します【文献8】。
これらの相乗効果は、黄ニキビにおける激しい炎症反応を説明する重要な機構です【文献2】。単一のサイトカインを標的とする介入では効果が限定的である理由も、この複雑な相互作用ネットワークの存在によって説明されます【文献2】。黄ニキビの病変部では、これらの相乗効果が重層的に作用し、炎症反応の自己増幅サイクルを形成します【文献2】。このサイトカインネットワークの包括的理解は、黄ニキビの病態生理を分子レベルで解明する上で不可欠です【文献2】。
活性酸素種と組織酸化障害
活性酸素種は、黄ニキビにおける組織障害の主要な媒介因子です【文献2】。好中球が炎症部位に到達すると、細胞膜に存在するNADPHオキシダーゼが活性化されます【文献2】。このオキシダーゼは、分子状酸素を電子受容体として、スーパーオキシドアニオンを生成します【文献2】。スーパーオキシドアニオンは、さらにスーパーオキシドジスムターゼによって過酸化水素へと変換されます。過酸化水素は、ミエロペルオキシダーゼの作用により、次亜塩素酸へと変換されます【文献2】。次亜塩素酸は、極めて強力な酸化作用を持ち、タンパク質、脂質、核酸を無差別に酸化します【文献2】。この酸化反応により、毛包上皮細胞、脂腺細胞、そして真皮の膠原線維が障害を受けます。
活性酸素種による脂質過酸化は、細胞膜の構造的完全性を破壊します【文献10】。細胞膜を構成するリン脂質の不飽和脂肪酸は、活性酸素種の攻撃を受けやすく、過酸化脂質へと変換されます【文献10】。過酸化脂質は、細胞膜の流動性を低下させ、膜タンパク質の機能を障害します。さらに、過酸化脂質は分解されて、4-ヒドロキシノネナールやマロンジアルデヒドといった反応性の高いアルデヒド化合物を生成します【文献10】。これらのアルデヒドは、タンパク質のアミノ基と反応し、タンパク質の構造と機能を不可逆的に変化させます【文献10】。黄ニキビの病変部では、これらの過酸化脂質と反応性アルデヒドの濃度が著しく上昇しており、広範な組織障害が生じています【文献10】。
活性酸素種は、マトリックスメタロプロテアーゼの発現も誘導します【文献2】。活性酸素種による細胞内シグナル伝達の活性化は、AP-1転写因子を活性化し、マトリックスメタロプロテアーゼ遺伝子の転写を促進します【文献2】。マトリックスメタロプロテアーゼは、真皮の膠原線維とエラスチン線維を分解する酵素であり、その活性増加は組織構造の破壊を加速します。また、活性酸素種は、組織修復に必要なコラーゲン合成を阻害し、線維芽細胞の機能を低下させます。このように、活性酸素種は、直接的な酸化障害と、間接的な酵素活性調節の両面から、黄ニキビにおける組織破壊に寄与します【文献2】【文献10】。活性酸素種による組織障害の理解は、黄ニキビにおける瘢痕形成のメカニズムを説明する上で重要です【文献10】。
好中球NADPHオキシダーゼによる活性酸素産生機構
好中球が産生する活性酸素種は、以下の段階を経て生成されます。この過程は、呼吸バーストと呼ばれ、好中球の主要な殺菌機構を構成します。
- NADPHオキシダーゼの活性化:好中球が炎症性刺激を受けると、細胞質に存在するp47phox、p67phox、p40phoxといった調節サブユニットが、細胞膜に存在するgp91phoxとp22phoxからなる触媒サブユニットに結合し、活性型酵素複合体を形成します【文献2】。
- スーパーオキシドアニオンの生成:活性化されたNADPHオキシダーゼは、NADPHから電子を取り出し、分子状酸素に転移させてスーパーオキシドアニオンを生成します。この反応は、酸素の一電子還元反応です【文献2】。
- 過酸化水素への変換:スーパーオキシドアニオンは、スーパーオキシドジスムターゼによって不均化反応を受け、過酸化水素と分子状酸素に変換されます【文献2】。
- 次亜塩素酸の生成:好中球の顆粒に含まれるミエロペルオキシダーゼが、過酸化水素と塩化物イオンから次亜塩素酸を生成します。次亜塩素酸は、活性酸素種の中で最も強力な酸化作用を持ちます【文献2】。
これらの活性酸素種は、協調的に作用して組織障害を引き起こします【文献2】。スーパーオキシドアニオンは、比較的反応性が低いものの、一酸化窒素と反応してペルオキシナイトライトを生成し、これが強力な酸化剤として作用します。過酸化水素は、細胞膜を通過して細胞内に侵入し、フェントン反応によってヒドロキシラジカルを生成します【文献2】。ヒドロキシラジカルは、あらゆる生体分子と反応する極めて強力な酸化剤です。次亜塩素酸は、タンパク質のメチオニンとシステイン残基を酸化し、タンパク質の機能を不可逆的に失活させます【文献2】。黄ニキビの病変部では、これらの活性酸素種が持続的に産生され、広範な組織酸化障害を引き起こします【文献2】。
活性酸素種による生体分子の酸化修飾
黄ニキビの病変部で産生される活性酸素種は、以下の生体分子に酸化修飾を引き起こします。これらの修飾は、細胞機能の障害と組織構造の破壊をもたらします。
- タンパク質のカルボニル化:活性酸素種は、タンパク質のアミノ酸側鎖、特にリジン、アルギニン、プロリン、トレオニンをカルボニル基に変換します。カルボニル化されたタンパク質は、正常な立体構造を失い、機能を喪失します【文献10】。
- 脂質の過酸化:細胞膜リン脂質とコレステロールの不飽和結合が酸化され、過酸化脂質が生成されます。この反応は連鎖的に進行し、広範な膜障害を引き起こします【文献10】。
- DNAの酸化損傷:ヒドロキシラジカルは、DNAの塩基とデオキシリボースを酸化し、8-ヒドロキシグアノシンなどの酸化損傷を生成します。DNA損傷は、細胞の増殖能力と修復能力を低下させます【文献2】。
- 膠原線維の断裂:活性酸素種は、膠原線維のペプチド結合を直接酸化切断し、また、マトリックスメタロプロテアーゼの発現を誘導して間接的にも膠原線維の分解を促進します【文献2】。
これらの酸化修飾は、累積的に作用して組織の構造的・機能的完全性を破壊します【文献2】【文献10】。特に、タンパク質のカルボニル化と脂質の過酸化は、細胞のエネルギー代謝と膜機能を著しく障害し、細胞死を誘導します【文献10】。また、膠原線維の酸化的断裂は、真皮の機械的強度を低下させ、組織の脆弱性を高めます【文献2】。黄ニキビの病変部では、これらの酸化修飾が広範に生じており、炎症が治癒した後も、不可逆的な組織障害として残存します【文献10】。活性酸素種による生体分子の酸化修飾の理解は、黄ニキビにおける組織破壊の分子基盤を明らかにします【文献2】【文献10】。
毛包内環境の変化と細菌増殖—アクネ菌の病原的役割
アクネ菌は、ヒト皮膚の常在菌であり、健常者の毛包内にも普遍的に存在します【文献1】。しかし、毛包内環境が変化すると、アクネ菌の増殖パターンと代謝活性が変化し、病原性を発揮するようになります【文献3】。正常な毛包では、アクネ菌の数は1毛包あたり数百から数千個程度であり、皮脂を栄養源として緩徐に増殖しています。この段階では、アクネ菌は宿主に対して病原性を示さず、むしろ他の病原性細菌の侵入を防ぐ役割を果たします【文献3】。しかし、微小面皰が形成され、毛包開口部が閉塞すると、毛包内の酸素分圧が低下し、嫌気性環境が形成されます【文献3】。アクネ菌は偏性嫌気性菌であるため、この環境変化は増殖に有利に作用し、菌数は急激に増加します【文献3】。
アクネ菌の増殖は、毛包内に蓄積した皮脂を栄養基質として進行します【文献3】。皮脂には、トリグリセリド、ワックスエステル、スクワレン、そしてコレステロールが含まれており、これらの脂質がアクネ菌の代謝を支えます【文献3】。特に、トリグリセリドは、アクネ菌が産生するリパーゼによって加水分解され、グリセロールと遊離脂肪酸に分解されます【文献3】。グリセロールはアクネ菌のエネルギー源となり、菌の増殖を促進します。一方、遊離脂肪酸は毛包内に蓄積し、毛包上皮に対して刺激作用を及ぼします【文献3】。閉鎖面皰内では、アクネ菌の数は1毛包あたり数百万個に達することがあり、これは正常毛包と比較して千倍以上の増加を示します【文献3】。この大量のアクネ菌が産生する代謝産物と酵素が、毛包内環境をさらに変化させ、炎症反応の開始を準備します【文献3】。
アクネ菌の病原性は、菌株によって異なることが明らかになっています【文献3】。アクネ菌は、系統樹解析により複数の系統型に分類され、痤瘡病変から分離される菌株は特定の系統型に偏ることが示されています【文献3】。特に、系統型IA1に分類される菌株は、炎症性痤瘡病変から高頻度で分離され、強い炎症誘導能を持つことが報告されています【文献3】。これらの病原性菌株は、より多くの病原性因子を産生し、宿主免疫系を強く刺激する特性を持ちます【文献3】。また、バイオフィルム形成能力も菌株間で異なり、バイオフィルムを形成する菌株は、宿主の免疫応答から保護され、長期間毛包内に残存する傾向があります【文献3】。このようなアクネ菌の多様性の理解は、黄ニキビ形成における細菌因子の役割を解明する上で重要です【文献3】。
アクネ菌が産生する病原性因子と生物学的作用
アクネ菌は、複数の病原性因子を産生し、これらが協調的に作用して宿主組織に障害を与えます【文献3】。最も重要な病原性因子の一つは、リパーゼです。アクネ菌のリパーゼは、複数のアイソフォームが存在し、それぞれ異なる基質特異性を持ちます【文献3】。これらのリパーゼは、皮脂中のトリグリセリドを加水分解し、遊離脂肪酸を生成します【文献3】。生成された遊離脂肪酸、特にオレイン酸やパルミチン酸といった飽和・不飽和脂肪酸は、毛包上皮のケラチノサイトに対して直接的な刺激作用を持ちます【文献3】。ケラチノサイトは、遊離脂肪酸に曝露されると、インターロイキン-1α、インターロイキン-8、そして腫瘍壊死因子-αといった炎症性サイトカインの産生を開始します【文献5】。この初期炎症応答が、赤ニキビから黄ニキビへの進行の起点となります【文献3】。
プロテアーゼもまた、重要な病原性因子です【文献3】。アクネ菌は、複数のプロテアーゼを産生し、これらが宿主タンパク質を分解します。特に、セリンプロテアーゼとメタロプロテアーゼは、毛包上皮の細胞間接着タンパク質を分解し、上皮バリアの完全性を損ないます【文献3】。また、これらのプロテアーゼは、補体成分や抗菌ペプチドを分解し、宿主の防御機構を回避します【文献3】。さらに、アクネ菌プロテアーゼは、プロインターロイキン-1βを直接切断し、成熟型インターロイキン-1βを生成する能力を持つことが報告されています【文献3】。この直接的なサイトカイン活性化は、インフラマソームを介さない炎症経路として機能し、炎症反応をさらに増幅します【文献3】。アクネ菌プロテアーゼによる宿主タンパク質の分解は、黄ニキビにおける毛包壁破綻の重要な機序の一つです【文献3】。
アクネ菌の細胞壁成分も、強力な免疫刺激活性を持ちます【文献2】。グラム陽性菌であるアクネ菌の細胞壁は、ペプチドグリカンとリポテイコ酸から構成されます【文献2】。ペプチドグリカンは、ケラチノサイトとマクロファージに発現するToll様受容体2とNOD2によって認識されます【文献2】。これらのパターン認識受容体の活性化は、NF-κBシグナル伝達経路を活性化し、炎症性サイトカインの産生を誘導します【文献2】。また、アクネ菌のペプチドグリカンは、補体系の副経路を活性化し、C5aなどの走化性因子を生成します【文献3】。リポテイコ酸もToll様受容体2のリガンドとして機能し、ペプチドグリカンと協調的に炎症反応を誘導します【文献2】。さらに、アクネ菌の細胞壁には、複数のタンパク質抗原が存在し、これらが獲得免疫系のT細胞を活性化します【文献3】。活性化されたT細胞は、インターフェロン-γとインターロイキン-17を産生し、マクロファージと好中球の活性化を促進します【文献2】。このように、アクネ菌の細胞壁成分は、自然免疫と獲得免疫の両方を活性化し、持続的な炎症反応を誘導します【文献2】【文献3】。
アクネ菌リパーゼによる皮脂分解機構
アクネ菌が産生するリパーゼは、以下の機序で皮脂を分解し、遊離脂肪酸を生成します。この過程が、毛包内環境の炎症性変化を開始します。
- リパーゼの分泌と活性化:アクネ菌は増殖過程で複数のリパーゼを細胞外に分泌します。これらのリパーゼは、毛包内のpHと温度条件下で最適な活性を示すように進化しています【文献3】。
- トリグリセリドの加水分解:リパーゼは、トリグリセリドのエステル結合を特異的に認識し、加水分解します。この反応により、グリセロール骨格から脂肪酸が遊離されます【文献3】。
- 遊離脂肪酸の蓄積:加水分解によって生成された遊離脂肪酸は、毛包内に蓄積します。閉鎖面皰では、遊離脂肪酸濃度が正常毛包の10倍以上に達することがあります【文献3】。
- ケラチノサイトの刺激:蓄積した遊離脂肪酸は、毛包上皮のケラチノサイトに作用し、細胞内シグナル伝達を活性化して炎症性サイトカインの産生を誘導します【文献3】【文献5】。
この一連の反応は、アクネ菌による炎症誘導の中心的メカニズムです【文献3】。遊離脂肪酸は、単なる代謝産物ではなく、能動的な炎症メディエーターとして機能します【文献3】。特に、オレイン酸は、ケラチノサイトのペルオキシソーム増殖因子活性化受容体を活性化し、炎症関連遺伝子の発現を調節します【文献3】。また、パルミチン酸は、Toll様受容体4のリガンドとしても機能し、NF-κB経路を活性化します【文献3】。このように、アクネ菌リパーゼによる皮脂分解は、単なる栄養獲得過程ではなく、炎症反応を惹起する戦略的な病原機構として理解されます【文献3】。
アクネ菌が産生するプロテアーゼの種類と基質特異性
アクネ菌は、以下の複数のプロテアーゼを産生し、それぞれが特異的な宿主タンパク質を標的とします。これらのプロテアーゼの協調作用が、毛包壁の破綻を促進します。
- セリンプロテアーゼ:トリプシン様の基質特異性を持ち、タンパク質のアルギニンとリジン残基の後ろのペプチド結合を切断します。このプロテアーゼは、細胞間接着タンパク質であるE-カドヘリンを分解し、上皮の結合を弱めます【文献3】。
- メタロプロテアーゼ:亜鉛イオンを補因子として利用し、膠原線維とエラスチン線維を分解します。このプロテアーゼは、毛包壁の構造タンパク質を標的とし、組織の機械的強度を低下させます【文献3】。
- システインプロテアーゼ:カテプシン様の活性を持ち、酸性環境下で最適な活性を示します。このプロテアーゼは、免疫グロブリンを分解し、抗体による細菌の中和を妨害します【文献3】。
- プロインターロイキン-1β切断酵素:特異的にプロインターロイキン-1βを認識して切断し、成熟型サイトカインを生成します。この活性により、アクネ菌はカスパーゼ-1を介さない炎症経路を活性化します【文献3】。
これらのプロテアーゼは、異なる機序で宿主防御を回避し、組織障害を促進します【文献3】。セリンプロテアーゼとメタロプロテアーゼは、物理的な組織破壊に直接寄与し、システインプロテアーゼは免疫回避を可能にします【文献3】。また、プロインターロイキン-1β切断酵素は、炎症反応を直接増幅する独自の機構を提供します【文献3】。黄ニキビの病変部では、これらのプロテアーゼが高濃度で存在し、毛包壁の構造的完全性を段階的に破壊します【文献3】。アクネ菌プロテアーゼの理解は、毛包壁破綻のメカニズムを分子レベルで説明する鍵となります【文献3】。
毛包内微小環境の物理化学的変化
微小面皰から炎症性病変への進行過程では、毛包内の物理化学的環境が劇的に変化します【文献3】。最も顕著な変化は、酸素分圧の低下です。正常な毛包では、開口部を通じて大気と接触しており、酸素が供給されます。しかし、面皰が形成され開口部が閉塞すると、酸素の供給が遮断されます【文献3】。毛包上皮細胞とアクネ菌の代謝によって酸素が消費されるため、毛包内の酸素分圧は急速に低下します【文献3】。閉鎖面皰内の酸素分圧は、大気中の酸素分圧の10分の1以下にまで低下することが測定されています【文献3】。この嫌気性環境は、偏性嫌気性菌であるアクネ菌の増殖に最適な条件を提供します【文献3】。一方、好気性菌や通性嫌気性菌の増殖は抑制され、結果としてアクネ菌が毛包内細菌叢の優占種となります【文献3】。
pH値の変化も重要な要因です【文献3】。正常な皮膚表面のpHは、弱酸性の5.5前後に維持されています。しかし、閉鎖面皰内では、アクネ菌の代謝によってプロピオン酸と酢酸が産生され、pHがさらに酸性側に傾きます【文献3】。アクネ菌は、グルコース代謝の最終産物として短鎖脂肪酸を産生し、これらが毛包内に蓄積します【文献3】。面皰内のpHは、4.5から5.0の範囲にまで低下することがあります【文献3】。この酸性環境は、アクネ菌自身の増殖には影響を与えませんが、ケラチノサイトの細胞膜に障害を与え、バリア機能を低下させます【文献3】。また、酸性pHは、アクネ菌が産生するプロテアーゼやリパーゼの活性を調節し、一部の酵素の活性を高めます【文献3】。さらに、酸性環境は補体系の活性化を促進し、炎症反応の増強に寄与します【文献3】。
浸透圧の上昇も、毛包内環境の特徴です【文献3】。閉鎖面皰内では、皮脂の蓄積、角質細胞の剥離、そしてアクネ菌の代謝産物の集積により、溶質濃度が上昇します【文献3】。この浸透圧上昇は、毛包壁に対して機械的な圧力を加え、上皮細胞の変性を促進します【文献3】。また、高浸透圧環境は、細胞内外の水分移動を変化させ、細胞の容積調節機構にストレスを与えます【文献3】。高浸透圧ストレスを受けた細胞は、ストレス応答遺伝子を発現し、炎症性サイトカインの産生が増加します【文献3】。さらに、浸透圧の上昇は毛包内圧を高め、毛包壁に対する機械的負荷を増大させます【文献3】。この機械的負荷は、既に炎症によって脆弱化した毛包壁の破綻を促進する要因となります【文献3】。このように、毛包内の物理化学的環境の変化は、アクネ菌の増殖促進と宿主組織の障害の両面から、黄ニキビ形成を促進します【文献3】。
酸素分圧低下がアクネ菌増殖に与える影響
毛包内の酸素分圧低下は、以下のメカニズムでアクネ菌の選択的増殖を促進します。この環境変化が、細菌叢の組成を劇的に変化させます。
- 嫌気性代謝経路の活性化:アクネ菌は、酸素非存在下でもグルコースを発酵によって代謝し、エネルギーを獲得できます。嫌気性環境では、発酵経路が優先的に利用され、プロピオン酸が主要な代謝産物として産生されます【文献3】。
- 好気性菌の増殖抑制:黄色ブドウ球菌や表皮ブドウ球菌といった好気性または通性嫌気性菌は、低酸素環境下では増殖速度が著しく低下します。この結果、細菌叢内でのアクネ菌の相対的比率が増加します【文献3】。
- 酸素毒性の回避:アクネ菌は、カタラーゼとスーパーオキシドジスムターゼといった酸素解毒酵素の活性が低いため、高酸素環境では活性酸素による障害を受けやすい特性を持ちます。嫌気性環境は、この酸素毒性から菌を保護します【文献3】。
- 毒素産生の増加:一部のアクネ菌株は、嫌気性条件下で特定の毒素や病原性因子の産生を増加させることが報告されています。この環境依存性の病原性発現が、炎症誘導能を高めます【文献3】。
これらの要因により、閉鎖面皰内ではアクネ菌が優占種となり、菌数は指数関数的に増加します【文献3】。正常毛包では多様な細菌叢が維持されていますが、面皰形成後はアクネ菌の単一培養に近い状態となります【文献3】。この細菌叢の多様性喪失は、宿主防御機構の観点からも不利に作用します【文献3】。多様な細菌叢は、相互に競合し、病原性菌の過剰増殖を抑制する効果を持ちますが、この効果が失われるためです【文献3】。酸素分圧低下による細菌叢変化の理解は、黄ニキビ形成における細菌学的基盤を説明します【文献3】。
毛包内pH変化と組織への影響
毛包内のpH低下は、以下の生物学的変化を引き起こし、炎症反応の準備と組織障害を促進します。pH変化は、単なる物理化学的変化ではなく、能動的な病態修飾因子として機能します。
- ケラチノサイトのバリア機能低下:pH 4.5以下の酸性環境は、ケラチノサイトの細胞膜を構成する脂質の相転移を引き起こし、膜の流動性と透過性を変化させます。この変化により、細胞のバリア機能が低下し、外来抗原の侵入が容易になります【文献3】。
- 酵素活性の調節:アクネ菌が産生するリパーゼとプロテアーゼの一部は、酸性pH下で最適活性を示します。pH低下により、これらの酵素の活性が増強され、皮脂分解と組織タンパク質分解が加速されます【文献3】。
- 酸感知受容体の活性化:ケラチノサイトは、ASIC(acid-sensing ion channel)と呼ばれる酸感知イオンチャネルを発現しています。細胞外pHの低下は、このチャネルを活性化し、細胞内カルシウムイオン濃度を上昇させます。この変化が、炎症性シグナル伝達を活性化します【文献3】。
- 補体系の活性化促進:補体系の副経路は、弱酸性環境下でより効率的に活性化されます。pH低下により、C3の自然加水分解速度が上昇し、補体カスケードが開始されやすくなります【文献3】。
これらのpH依存性変化は、毛包内環境を炎症誘導型へと変化させます【文献3】。特に、ケラチノサイトのバリア機能低下と酸感知受容体の活性化は、炎症性サイトカインの産生を誘導する重要なトリガーとなります【文献3】。また、酵素活性の増強は、組織障害を加速し、炎症反応をさらに増幅します【文献3】。毛包内pH変化の理解は、アクネ菌感染が炎症反応を惹起する分子機構を説明する上で重要です【文献3】。
アクネ菌バイオフィルム形成と宿主応答の複雑化
バイオフィルムは、細菌が産生する細胞外マトリックスに包埋された細菌集団として定義されます【文献3】。アクネ菌も、毛包内でバイオフィルムを形成する能力を持ち、この構造が炎症反応を複雑化させます【文献3】。バイオフィルム内のアクネ菌は、浮遊状態の菌とは異なる遺伝子発現パターンを示し、代謝活性と増殖速度が低下します【文献3】。この低代謝状態は、細菌を宿主の免疫攻撃から保護する効果を持ちます【文献3】。好中球は、バイオフィルムを貪食することが困難であり、また、バイオフィルム内部への抗菌物質の浸透も制限されます【文献3】。さらに、バイオフィルムを構成する細胞外マトリックスは、好中球が放出するプロテアーゼや活性酸素種を吸収し、その作用を減弱させます【文献3】。
アクネ菌のバイオフィルムは、主に多糖類、タンパク質、そして細胞外DNAから構成されます【文献3】。多糖類成分は、細菌細胞を物理的に結合し、三次元構造を形成します。タンパク質成分には、接着因子と酵素が含まれており、これらが宿主組織への付着とバイオフィルムの維持に寄与します【文献3】。細胞外DNAは、バイオフィルムの構造的完全性を高めるとともに、好中球が放出するリソソーム酵素を阻害する効果を持ちます【文献3】。バイオフィルム内のアクネ菌は、栄養勾配と酸素勾配に曝されており、外層と内層で異なる代謝状態を示します【文献3】。外層の細菌は比較的活発に増殖しますが、内層の細菌は休眠状態に近く、代謝活性が極めて低くなります【文献3】。この不均一性が、バイオフィルムの強靭性と持続性を支えます【文献3】。
バイオフィルム形成は、宿主の免疫応答を質的に変化させます【文献3】。浮遊状態のアクネ菌に対しては、好中球の貪食作用が効果的に機能しますが、バイオフィルムに対しては、好中球は細胞外に活性酸素種とプロテアーゼを放出する応答パターンに切り替わります【文献3】。この応答パターンの変化は、周囲組織への副次的障害を増大させます【文献3】。また、バイオフィルムは、マクロファージを慢性的に活性化し、持続的な炎症性サイトカイン産生を誘導します【文献3】。さらに、バイオフィルム由来の細菌成分は、樹状細胞を活性化し、Th17型の免疫応答を誘導します【文献3】。Th17細胞が産生するインターロイキン-17は、好中球の動員をさらに増強し、炎症反応を慢性化させます【文献2】【文献3】。このように、バイオフィルム形成は、急性炎症を慢性炎症へと移行させ、黄ニキビの持続と増悪に寄与します【文献3】。
バイオフィルムの構造的特徴と機能的意義
アクネ菌が形成するバイオフィルムは、以下の構造的特徴を持ち、それぞれが宿主防御からの回避に寄与します。これらの特徴が、バイオフィルムの強靭性を支えます。
- 三次元マトリックス構造:細菌細胞は、多糖類とタンパク質からなる細胞外マトリックスに包埋され、密集したマイクロコロニーを形成します。この構造により、物理的な保護効果が得られます【文献3】。
- 水チャネルの形成:バイオフィルム内部には、栄養と代謝産物の輸送を可能にする水チャネルが形成されます。このチャネル系が、バイオフィルム内部の細菌への栄養供給を維持します【文献3】。
- 濃度勾配の存在:バイオフィルムの外層から内層にかけて、酸素、栄養素、代謝産物の濃度勾配が形成されます。この勾配により、細菌は異なる代謝状態を示し、全体として環境変化への抵抗性を獲得します【文献3】。
- 細胞外DNA網:死滅した細菌から放出されたDNAが、バイオフィルムマトリックスの構造成分として組み込まれます。このDNA網は、プロテアーゼを捕捉し、その活性を中和する効果を持ちます【文献3】。
これらの構造的特徴により、バイオフィルムは宿主の免疫攻撃に対して高い抵抗性を示します【文献3】。特に、細胞外マトリックスによる物理的保護と、細胞外DNAによる酵素阻害効果は、好中球とマクロファージの殺菌活動を著しく減弱させます【文献3】。また、バイオフィルム内部の低代謝状態の細菌は、免疫系による認識を回避し、長期間生存することが可能です【文献3】。バイオフィルム形成の理解は、黄ニキビにおける慢性炎症と組織破壊の持続機構を説明します【文献3】。
バイオフィルムに対する宿主免疫応答の特徴
アクネ菌のバイオフィルムに対して、宿主免疫系は以下の応答パターンを示します。これらの応答は、浮遊状態の細菌に対する応答とは質的に異なります。
- 好中球のフラストレーション応答:好中球は、バイオフィルムを効率的に貪食できないため、細胞外に大量の活性酸素種とプロテアーゼを放出します。この応答は、周囲の正常組織に広範な障害を与えます【文献3】。
- マクロファージの持続的活性化:バイオフィルムは、マクロファージを慢性的に刺激し、M1型の炎症促進性表現型を維持させます。このマクロファージは、継続的に炎症性サイトカインを産生します【文献3】。
- Th17型免疫応答の誘導:バイオフィルム由来の細菌成分は、樹状細胞を介してTh17細胞の分化を誘導します。Th17細胞が産生するインターロイキン-17は、好中球の動員と活性化を増強し、炎症を増幅します【文献2】【文献3】。
- NETsの形成:好中球は、バイオフィルムに対してNETs(neutrophil extracellular traps)と呼ばれるDNA網を放出します。NETsは細菌を捕捉する効果を持ちますが、同時に組織障害も引き起こします【文献3】。
これらの免疫応答パターンは、バイオフィルム感染の特徴であり、浮遊細菌感染とは異なる病態を形成します【文献3】。特に、好中球のフラストレーション応答は、黄ニキビにおける広範な組織破壊の重要な機序です【文献3】。また、Th17型免疫応答の誘導は、炎症の慢性化と再発傾向の原因となります【文献2】【文献3】。バイオフィルムに対する宿主応答の理解は、黄ニキビの複雑な免疫病理学的メカニズムを解明する鍵となります【文献3】。
免疫応答と好中球浸潤—炎症性サイトカインによる膿形成
黄ニキビにおける膿の形成は、好中球の大量動員と集積によって実現されます【文献2】。この過程は、炎症性サイトカイン、特にインターロイキン-8が中心的な役割を果たす、高度に組織化された免疫応答です【文献2】。毛包内でアクネ菌が増殖し、炎症性メディエーターが産生されると、これらのシグナルは血管内皮細胞に到達し、内皮細胞の活性化を誘導します【文献2】。活性化された血管内皮細胞は、表面に接着分子を発現し、血流中を循環する好中球を捕捉します【文献2】。捕捉された好中球は、血管壁を通過して組織内に遊走し、炎症部位へと集積します【文献2】。この一連のプロセスは、白血球接着カスケードと呼ばれ、複数の段階から構成されます【文献2】。
好中球の動員は、ケモカイン濃度勾配に沿って進行します【文献2】。インターロイキン-8は、最も強力な好中球走化因子であり、炎症部位で高濃度に産生されます【文献2】。このケモカインは、拡散によって周囲組織に広がり、血管から炎症部位へと向かう濃度勾配を形成します【文献2】。好中球は、細胞表面に発現するCXCR1とCXCR2受容体を介してインターロイキン-8を感知し、濃度勾配の高い方向へと遊走します【文献2】。この走化性応答により、好中球は効率的に炎症部位へと誘導されます【文献2】。黄ニキビの病変部では、インターロイキン-8濃度が正常皮膚と比較して数百倍に上昇しており、これが大量の好中球動員を可能にします【文献2】。集積した好中球は、炎症部位で活性化され、貪食作用、活性酸素産生、そしてプロテアーゼ放出といった殺菌機能を発揮します【文献2】。
好中球の集積は、時間依存的に進行します【文献4】。赤ニキビの初期段階では、好中球の数は比較的少なく、マクロファージとリンパ球が主要な浸潤細胞です【文献4】。しかし、炎症が進行し、インターロイキン-8の産生が増加するにつれて、好中球の浸潤が加速されます【文献2】。黄ニキビの段階では、好中球が浸潤細胞の大部分を占めるようになり、その数は1立方ミリメートルあたり数百万個に達します【文献2】。このような高密度の好中球集積は、膿疱の特徴的な所見であり、膿の主要成分を構成します【文献2】。集積した好中球の多くは、短時間のうちにアポトーシスまたは壊死に至り、その残骸が膿として観察されます【文献2】。好中球の死滅は、細胞内酵素と核物質を細胞外に放出し、これがさらなる組織障害と炎症反応の増幅を引き起こします【文献2】。このように、好中球の動員、集積、活性化、そして死滅という一連のプロセスが、黄ニキビにおける膿疱形成の本質的メカニズムを構成します【文献2】。
白血球接着カスケードと好中球の血管外遊出
好中球の組織内遊走は、白血球接着カスケードと呼ばれる多段階プロセスを経て実現されます【文献2】。第一段階は、ローリングと呼ばれる現象です。炎症性サイトカインによって活性化された血管内皮細胞は、P-セレクチンとE-セレクチンを細胞表面に発現します【文献2】。これらのセレクチンは、好中球表面のセレクチンリガンドと弱い結合を形成し、血流中の好中球を血管壁に捕捉します【文献2】。捕捉された好中球は、血流によって引きずられながら、血管内皮上を転がるように移動します【文献2】。このローリング状態では、好中球の移動速度は血流速度よりも著しく遅くなり、内皮細胞が提示するケモカインを感知する機会が与えられます【文献2】。
第二段階は、活性化と強固な接着です【文献2】。ローリング中の好中球は、血管内皮細胞が表面に提示するインターロイキン-8を受容体で認識します【文献2】。インターロイキン-8の結合は、好中球内部のシグナル伝達を活性化し、インテグリン分子の構造変化を誘導します【文献2】。インテグリンは、不活性型から活性型へと構造変化することで、リガンドへの親和性が数百倍に上昇します【文献2】。活性化されたインテグリンは、血管内皮細胞上のICAM-1とVCAM-1に強固に結合し、好中球を血管壁に固定します【文献2】。この段階で、好中球のローリングは停止し、血管内皮に平坦に広がるように接着します【文献2】。この形態変化は、スプレッディングと呼ばれ、好中球が血管壁を通過する準備段階となります【文献2】。
第三段階は、血管外遊出です【文献2】。血管内皮に強固に接着した好中球は、内皮細胞間の接合部を認識し、この部位から血管壁を通過します【文献2】。好中球は、PECAM-1やCD99といった接合部に局在する分子を利用して、内皮細胞層を通過します【文献2】。内皮細胞層を通過した好中球は、次に基底膜を突破する必要があります【文献2】。好中球は、マトリックスメタロプロテアーゼとエラスターゼを放出し、基底膜を構成するコラーゲンIV型とラミニンを部分的に分解します【文献2】。この酵素的分解により、好中球は基底膜に通過孔を形成し、血管外の組織内へと移動します【文献2】。血管外遊出を完了した好中球は、組織内でインターロイキン-8の濃度勾配を感知し、炎症部位へと向かって遊走を開始します【文献2】。黄ニキビの病変部では、このプロセスが連続的に生じており、大量の好中球が毛包周囲に集積します【文献2】。
血管内皮細胞の活性化と接着分子の発現誘導
炎症性サイトカインによる血管内皮細胞の活性化は、以下の段階を経て接着分子の発現を誘導します。この過程が、好中球の接着と遊走を可能にします。
- 初期応答(0-2時間):インターロイキン-1βと腫瘍壊死因子-αが内皮細胞に作用すると、細胞内に貯蔵されていたP-セレクチンが、数分以内に細胞表面に移動します。この迅速な応答により、早期の好中球ローリングが開始されます【文献2】。
- 中期応答(2-6時間):転写因子NF-κBとAP-1の活性化により、E-セレクチン遺伝子の転写が誘導されます。E-セレクチンタンパク質が合成され、細胞表面に発現されることで、好中球のローリングがさらに効率化されます【文献2】。
- 後期応答(6-24時間):ICAM-1とVCAM-1の遺伝子発現が誘導され、これらの接着分子が細胞表面に高密度で発現されます。この段階で、好中球の強固な接着が可能となります【文献2】。
- ケモカイン提示:内皮細胞は、インターロイキン-8を細胞表面に結合させ、ローリング中の好中球に提示します。この提示機構により、好中球は効率的にケモカインを感知し、活性化されます【文献2】。
これらの時間依存的な接着分子発現パターンは、好中球動員の効率を最大化します【文献2】。初期のP-セレクチン発現は迅速な応答を可能にし、中期のE-セレクチン発現は持続的なローリングを維持し、後期のICAM-1発現は強固な接着を実現します【文献2】。黄ニキビの病変部では、これらの接着分子がすべて高レベルで発現しており、好中球の大量動員が持続的に進行します【文献2】。血管内皮細胞の活性化の理解は、好中球集積のメカニズムを分子レベルで説明します【文献2】。
好中球の血管外遊出における細胞間相互作用
好中球が血管壁を通過する過程では、以下の細胞間相互作用が協調的に機能します。これらの相互作用が、効率的な血管外遊出を可能にします。
- セレクチン-リガンド相互作用:血管内皮細胞上のE-セレクチンとP-セレクチンが、好中球表面のPSGL-1(P-selectin glycoprotein ligand-1)と結合し、好中球のローリングを媒介します【文献2】。
- ケモカイン-受容体相互作用:内皮細胞が提示するインターロイキン-8が、好中球のCXCR1およびCXCR2受容体に結合し、細胞内シグナル伝達を活性化します【文献2】。
- インテグリン-ICAM相互作用:活性化された好中球のLFA-1(リンパ球機能関連抗原1)とMac-1が、内皮細胞のICAM-1に強固に結合し、好中球を血管壁に固定します【文献2】。
- PECAM-1の同種結合:好中球と内皮細胞の両方に発現するPECAM-1分子が、同種結合を形成し、好中球の内皮細胞間接合部通過を促進します【文献2】。
これらの相互作用は、時系列的に協調して機能し、好中球の血管外遊出を段階的に進行させます【文献2】。各段階での相互作用の失敗は、好中球動員の効率を低下させますが、黄ニキビの病変部では、すべての相互作用が最適に機能しており、大量の好中球遊出が実現されます【文献2】。血管外遊出における細胞間相互作用の理解は、好中球集積の分子機構を詳細に説明します【文献2】。
好中球の活性化と殺菌機能の発現
組織内に遊走した好中球は、炎症部位で完全に活性化され、殺菌機能を発揮します【文献2】。好中球の活性化は、複数の刺激によって誘導されます【文献2】。まず、インターロイキン-8とC5aといった走化因子が、好中球を活性化します【文献2】。これらの因子の受容体への結合は、細胞内カルシウムイオン濃度の上昇とプロテインキナーゼCの活性化を誘導します【文献2】。さらに、アクネ菌の細胞壁成分が好中球表面のToll様受容体2に結合し、追加の活性化シグナルを提供します【文献2】。また、好中球が組織内の細胞外マトリックスタンパク質と接触することも、インテグリンを介した活性化シグナルを生成します【文献2】。これらの複合的な刺激により、好中球は最大限に活性化された状態となります【文献2】。
活性化された好中球は、まず貪食作用を試みます【文献2】。好中球は、アクネ菌を認識するために、複数の受容体を利用します【文献2】。オプソニン化された細菌は、Fcγ受容体と補体受容体によって効率的に認識されます【文献2】。血清中の抗体とC3bが細菌表面を覆うことで、オプソニン化が達成されます【文献2】。また、好中球は、マンノース受容体やスカベンジャー受容体を介して、オプソニン非依存的にも細菌を認識できます【文献2】。認識された細菌は、好中球の細胞膜に包み込まれ、ファゴソームと呼ばれる細胞内小胞に取り込まれます【文献2】。ファゴソームは、リソソームと融合してファゴリソソームを形成し、内部の細菌を殺菌します【文献2】。ファゴリソソーム内では、NADPHオキシダーゼが活性酸素種を産生し、同時にリソソーム顆粒から放出された抗菌ペプチドとプロテアーゼが作用します【文献2】。
しかし、黄ニキビの病変部では、好中球の貪食作用は必ずしも成功しません【文献3】。アクネ菌がバイオフィルムを形成している場合、好中球は細菌を効率的に貪食できません【文献3】。また、アクネ菌の数が好中球の処理能力を超えている場合も、貪食作用は不完全となります【文献3】。このような状況では、好中球は細胞外に殺菌因子を放出する戦略に切り替えます【文献2】。この細胞外殺菌機構は、フラストレーション貪食とも呼ばれ、活性酸素種とプロテアーゼが細胞外に大量放出されます【文献2】。細胞外に放出された殺菌因子は、細菌だけでなく周囲の宿主組織にも障害を与えます【文献2】。この非特異的な組織障害が、黄ニキビにおける広範な毛包壁破壊と真皮障害の主要な機序となります【文献2】。さらに、好中球はNETsを形成し、DNAとヒストンからなる網状構造を細胞外に放出します【文献2】。NETsは細菌を物理的に捕捉する効果を持ちますが、同時に組織に対しても毒性を示します【文献2】。
好中球の活性化を誘導するシグナル分子
組織内に遊走した好中球は、以下のシグナル分子によって活性化され、殺菌機能を発現します。これらのシグナルは、相乗的に作用して好中球を最大限に活性化します。
- インターロイキン-8:好中球のCXCR受容体に結合し、細胞内カルシウム動員とMAPK活性化を誘導します。この活性化により、好中球の走化性、貪食能、そして活性酸素産生能が増強されます【文献2】。
- 補体C5a:好中球のC5a受容体に結合し、Gタンパク質共役型シグナル伝達を活性化します。C5aは、好中球の脱顆粒を促進し、リソソーム酵素の放出を誘導します【文献2】。
- 顆粒球マクロファージコロニー刺激因子(GM-CSF):好中球の生存期間を延長し、アポトーシスを遅延させます。これにより、炎症部位での好中球の活動時間が延長されます【文献2】。
- インターフェロン-γ:Th1細胞から産生され、好中球の活性酸素産生能とプロテアーゼ放出を増強します。また、好中球とマクロファージの協調作用を促進します【文献2】。
これらのシグナル分子は、黄ニキビの病変部で高濃度に存在し、好中球を持続的に活性化状態に維持します【文献2】。特に、インターロイキン-8とC5aの相乗効果は、好中球の殺菌活性を最大化します【文献2】。また、GM-CSFによる生存期間延長は、好中球が長時間にわたって組織内で活動することを可能にし、これが持続的な組織障害につながります【文献2】。好中球活性化シグナルの理解は、膿疱形成における好中球の役割を分子レベルで説明します【文献2】。
好中球が放出する殺菌因子とその作用機序
活性化された好中球は、以下の殺菌因子を細胞外に放出します。これらの因子は、細菌殺滅と組織障害の両方に寄与します。
- 活性酸素種:NADPHオキシダーゼが産生するスーパーオキシドアニオン、過酸化水素、次亜塩素酸は、細菌の細胞膜とタンパク質を酸化し、殺菌効果を発揮します。同時に、これらは宿主組織の脂質とタンパク質も酸化します【文献2】。
- 好中球エラスターゼ:セリンプロテアーゼであり、エラスチン線維と膠原線維を分解します。細菌の表層タンパク質も分解しますが、毛包壁と真皮の構造タンパク質も同様に破壊します【文献2】。
- カテプシンG:システインプロテアーゼであり、広範な基質特異性を持ちます。細菌の細胞壁ペプチドグリカンを分解するとともに、宿主の細胞外マトリックスタンパク質も分解します【文献2】。
- ミエロペルオキシダーゼ:過酸化水素と塩化物イオンから次亜塩素酸を生成します。次亜塩素酸は、極めて強力な酸化作用を持ち、細菌と宿主細胞を無差別に障害します【文献2】。
- 抗菌ペプチド:ディフェンシンとカテリシジンは、細菌の細胞膜に孔を形成し、浸透圧溶解を引き起こします。これらのペプチドは、グラム陽性菌とグラム陰性菌の両方に対して殺菌活性を示します【文献2】。
これらの殺菌因子の細胞外放出は、黄ニキビにおける組織破壊の主要な機序です【文献2】。特に、活性酸素種とプロテアーゼの組み合わせは、毛包壁の膠原線維とエラスチン線維を効果的に分解します【文献2】。また、ミエロペルオキシダーゼが産生する次亜塩素酸は、タンパク質のカルボニル化を引き起こし、不可逆的な組織障害をもたらします【文献2】。好中球が放出する殺菌因子の理解は、黄ニキビにおける膿形成と組織破壊のメカニズムを統合的に説明します【文献2】。
好中球の死滅と膿の構成成分形成
炎症部位に集積した好中球の多くは、短時間のうちに死滅します【文献2】。好中球の寿命は、血中では約8時間、組織内では1-2日程度ですが、激しい炎症環境下ではさらに短縮されます【文献2】。好中球の死滅は、主にアポトーシスと壊死の二つの経路によって生じます【文献2】。正常な条件下では、好中球は計画的細胞死であるアポトーシスによって死滅します【文献2】。アポトーシスを起こした好中球は、細胞膜の完全性を維持したまま断片化し、マクロファージによって速やかに貪食されます【文献2】。このプロセスは、炎症反応を増幅させずに好中球を除去する効率的な機構です【文献2】。しかし、黄ニキビの病変部では、激しい炎症環境と組織障害により、多くの好中球が壊死に至ります【文献2】。
壊死は、細胞膜の破綻を伴う非計画的細胞死です【文献2】。活性酸素種とプロテアーゼに曝露された好中球は、細胞膜が障害され、内容物が細胞外に漏出します【文献2】。壊死した好中球からは、リソソーム酵素、ミエロペルオキシダーゼ、そして核物質が放出されます【文献2】。核物質には、DNAとヒストンが含まれており、これらが膿の粘稠性を高めます【文献2】。また、壊死細胞から放出されるDAMPs(damage-associated molecular patterns)は、周囲の免疫細胞を刺激し、さらなる炎症反応を誘導します【文献2】。特に、高移動度グループボックス1タンパク質(HMGB1)とS100タンパク質は、強力な炎症惹起活性を持ち、炎症の自己増幅に寄与します【文献2】。このように、好中球の壊死は、炎症反応をさらに増幅させる悪循環を形成します【文献2】。
死滅した好中球の残骸が、膿の主要成分を構成します【文献2】。膿は、外観上は黄白色の粘稠な液体ですが、顕微鏡的には、断片化した好中球の核、細胞質顆粒、細胞膜片、そして細胞外に放出された酵素とDNAの混合物として観察されます【文献2】。膿中の細胞数は、1マイクロリットルあたり数万から数十万個に達し、その大部分は死滅した好中球です【文献2】。また、膿には、壊死したケラチノサイト、アクネ菌とその断片、そして血清成分も含まれています【文献2】。膿のpHは、リソソーム酵素の作用と代謝産物の蓄積により、弱酸性を示します【文献2】。また、膿中の酵素活性は高く、タンパク質分解活性と脂質分解活性が検出されます【文献2】。この酵素活性は、膿疱が破裂した際に周囲組織への拡大障害を引き起こす要因となります【文献2】。膿の形成は、黄ニキビの最も特徴的な病理学的所見であり、好中球の動員、活性化、そして死滅という一連のプロセスの最終的な帰結として理解されます【文献2】。
好中球のアポトーシスと壊死の決定因子
炎症部位における好中球の運命は、以下の因子によって決定されます。これらの因子が、アポトーシスと壊死のバランスを制御します。
- 生存シグナルの有無:GM-CSFやG-CSFといった生存因子が存在する場合、好中球はアポトーシスが遅延され、活動期間が延長されます。しかし、黄ニキビの病変中心部では、これらの因子の濃度が相対的に低く、好中球の早期死滅が生じます【文献2】。
- 酸化ストレスの強度:強い酸化ストレス環境では、好中球のミトコンドリアと細胞膜が直接障害され、壊死が誘導されます。活性酸素種の濃度が閾値を超えると、計画的なアポトーシス経路は機能せず、壊死が優位となります【文献2】。
- プロテアーゼ曝露:細胞外プロテアーゼの高濃度曝露は、好中球の細胞膜タンパク質を分解し、膜の完全性を破壊します。この物理的障害により、壊死が誘導されます【文献2】。
- エネルギー枯渇:好中球の激しい代謝活動は、ATPを急速に消費します。炎症部位での低酸素環境と栄養不足により、エネルギー枯渇が生じ、これが壊死を促進します【文献2】。
これらの因子は、黄ニキビの病変部で複合的に作用し、好中球の壊死を優位にします【文献2】。特に、病変中心部の低酸素環境と高濃度の酸化ストレスは、好中球の計画的死滅機構を破綻させ、壊死を誘導します【文献2】。壊死優位の細胞死は、炎症反応のさらなる増幅を招き、膿疱形成と組織破壊を加速させます【文献2】。好中球の死滅機序の理解は、膿の形成過程を細胞生物学的に説明します【文献2】。
膿の物理化学的性状と生物学的活性
黄ニキビの膿は、以下の物理化学的性状と生物学的活性を示します。これらの特性が、膿疱の臨床的特徴を決定します。
- 粘稠性:死滅した好中球から放出されたDNAとヒストンが、高分子網状構造を形成し、膿に粘稠性を付与します。この粘稠性により、膿は容易には流出せず、毛包内に貯留します【文献2】。
- 酵素活性:膿中には、エラスターゼ、カテプシンG、ミエロペルオキシダーゼといった多数の酵素が高濃度で存在し、活性を保持しています。これらの酵素は、膿疱破裂時に周囲組織を障害する能力を持ちます【文献2】。
- 炎症惹起活性:膿中のDAMPs、特にHMGBと1S100タンパク質は、周囲の免疫細胞を刺激し、新たな炎症反応を誘導します。この活性により、膿疱の破裂は炎症の拡大を招きます【文献2】。
- pH:膿のpHは5.0-5.5の弱酸性を示し、この酸性環境は周囲組織に対して刺激作用を持ちます。また、一部の酵素の活性を増強します【文献2】。
- 浸透圧:高濃度のタンパク質と核酸の存在により、膿の浸透圧は血漿よりも高く、これが膿疱内への水分引き込みを促進し、膿疱の膨張を維持します【文献2】。
これらの物理化学的性状は、黄ニキビの臨床像と病態進行に直接影響します【文献2】。粘稠性の高い膿は、自然排出が困難であり、毛包内に長期間貯留します【文献2】。酵素活性と炎症惹起活性は、膿疱破裂時の周囲組織への障害拡大を説明します【文献2】。また、高浸透圧は膿疱の膨張を維持し、毛包壁への機械的負荷を増大させます【文献2】。膿の性状の理解は、黄ニキビにおける膿疱の形成と維持のメカニズムを包括的に説明します【文献2】。
毛包壁破裂と真皮層への炎症拡大—組織障害のメカニズム
毛包壁の破裂は、黄ニキビの病態において決定的な転換点を示します【文献4】。この段階で、炎症反応は毛包という限定された空間から、周囲の真皮組織へと拡大します【文献4】。毛包壁の破裂は、複合的な要因によって引き起こされます。第一に、好中球とアクネ菌が産生するプロテアーゼによる酵素的分解が、毛包壁の構造タンパク質を段階的に破壊します【文献3】。第二に、活性酸素種による酸化障害が、膠原線維とエラスチン線維の架橋結合を切断し、組織の機械的強度を低下させます【文献2】。第三に、毛包内圧の上昇が、脆弱化した毛包壁に対して持続的な機械的負荷を加えます【文献3】。これらの因子が統合的に作用することで、毛包壁は最終的に破綻します【文献4】。
毛包壁が破裂する位置は、組織学的に特定のパターンを示します【文献4】。最も頻繁に破裂が生じるのは、毛包の中下部、すなわち脂腺開口部よりも深い位置です【文献4】。この部位では、炎症反応が最も激しく、好中球の集積密度が最大となります【文献4】。また、この部位の毛包壁は、他の部位と比較して相対的に薄く、機械的強度が低い構造的特徴を持ちます【文献4】。破裂部位では、組織学的に基底膜の完全な消失と、毛包上皮の広範な壊死が観察されます【文献4】。破裂した毛包壁の縁は、不規則な形状を示し、炎症性細胞が密集しています【文献4】。この破裂部位を通じて、毛包内容物が真皮層へと流出します【文献4】。流出する物質には、大量のアクネ菌とその代謝産物、死滅した好中球の残骸、リソソーム酵素、活性酸素種、そして角質と皮脂が含まれます【文献3】【文献4】。
毛包内容物の真皮流出は、激しい異物反応を惹起します【文献3】。真皮層に常在するマクロファージは、流出したアクネ菌成分と細胞残骸を認識し、即座に活性化されます【文献3】。活性化されたマクロファージは、インターロイキン-1β、インターロイキン-6、腫瘍壊死因子-αといった炎症性サイトカインを大量に産生します【文献2】。また、真皮の肥満細胞も脱顆粒し、ヒスタミンとトリプターゼを放出します【文献3】。ヒスタミンは血管透過性を急激に亢進させ、血漿成分の組織内漏出を促進します【文献3】。この結果、破裂部位の周囲には著明な浮腫が形成されます【文献3】。さらに、流出した角質と皮脂は、真皮内で異物肉芽腫を形成します【文献9】。異物肉芽腫では、多核巨細胞が出現し、異物を貪食しようとしますが、角質と皮脂の完全な分解は困難です【文献9】。この慢性的な異物反応が、炎症の持続と瘢痕形成の基盤となります【文献9】。
毛包壁の構造的破綻に至る段階的プロセス
毛包壁の破綻は、瞬間的な事象ではなく、段階的に進行するプロセスです【文献4】。第一段階では、毛包上皮細胞の変性が開始されます。炎症性メディエーターと活性酸素種に曝露された上皮細胞は、細胞質の空胞化と核の濃縮を示します【文献4】。この段階では、細胞膜の完全性はまだ維持されており、基底膜も連続しています【文献4】。しかし、細胞内のミトコンドリア機能は既に障害されており、エネルギー産生が低下しています【文献4】。第二段階では、基底膜の部分的断裂が生じます【文献4】。好中球エラスターゼとマトリックスメタロプロテアーゼ-9は、基底膜を構成するIV型膠原とラミニンを特異的に分解します【文献2】【文献4】。基底膜に生じた微小な断裂部位からは、炎症性細胞が毛包内腔に侵入し始めます【文献4】。
第三段階では、上皮層の広範な壊死が生じます【文献4】。持続的な酸化ストレスとプロテアーゼ曝露により、上皮細胞は大規模に壊死に陥ります【文献4】。壊死した細胞は、細胞膜が破綻し、細胞内容物が周囲に放出されます【文献4】。この細胞内容物には、DAMPsが含まれており、これがさらなる炎症反応を誘導します【文献2】。組織学的には、この段階で毛包壁の連続性が広範に失われ、毛包内腔と真皮層の境界が不明瞭となります【文献4】。第四段階では、毛包壁の完全な破綻が生じます【文献4】。毛包内圧の上昇と組織の機械的強度の喪失により、残存していた毛包壁の断片が崩壊します【文献4】。この段階で、毛包内容物が真皮層へと大量に流出し、炎症は毛包の境界を越えて拡大します【文献4】。破裂部位の辺縁には、好中球と壊死組織が混在した膿瘍様構造が形成されます【文献4】。
毛包壁破綻の時間経過は、個々の病変によって異なりますが、典型的には赤ニキビの出現から数日から1週間程度で生じます【文献4】。破綻の速度は、炎症反応の強度、アクネ菌の病原性、そして個体の免疫応答性によって影響されます【文献3】。強い炎症反応を示す病変では、毛包壁破綻がより早期に、より広範に生じます【文献4】。また、系統型IA1のアクネ菌に感染した病変では、より激しい炎症と早期の毛包壁破綻が観察されます【文献3】。個体差としては、マトリックスメタロプロテアーゼの発現量が高い体質では、毛包壁破綻が生じやすい傾向があります【文献9】。このような段階的プロセスの理解は、黄ニキビにおける組織破壊の時間的・空間的パターンを説明します【文献4】。
毛包壁を構成する組織成分とその脆弱性
毛包壁は、以下の組織成分から構成されており、それぞれが炎症性障害に対して特異的な脆弱性を持ちます。これらの成分の段階的破壊が、毛包壁破綻を引き起こします。
- 毛包上皮:重層扁平上皮からなる毛包の内層であり、ケラチノサイトで構成されます。炎症性サイトカインと活性酸素種に対して最も脆弱であり、早期に変性と壊死を示します【文献4】。
- 基底膜:IV型膠原、ラミニン、パールカン、ニドゲンから構成される薄い膜構造です。マトリックスメタロプロテアーゼと好中球エラスターゼによって効率的に分解され、毛包壁破綻の起点となります【文献4】。
- 結合組織鞘:毛包の外層を構成する膠原線維とエラスチン線維の束です。プロテアーゼによる酵素的分解と活性酸素種による酸化的切断の両方を受け、機械的強度が段階的に低下します【文献4】。
- 血管網:毛包周囲には豊富な毛細血管が分布しています。炎症により血管透過性が亢進し、浮腫形成に寄与します。また、血管内皮の障害は、血栓形成と局所虚血を引き起こし、組織壊死を増悪させます【文献3】。
これらの組織成分の中で、基底膜の破綻が最も重要な転換点となります【文献4】。基底膜は、上皮層と結合組織を分離する境界構造であり、この膜の連続性が失われることで、炎症は真皮層へと拡大します【文献4】。特に、IV型膠原の分解は、基底膜の構造的完全性を決定的に損ないます【文献4】。また、結合組織鞘の膠原線維とエラスチン線維の破壊は、毛包壁の引張強度を低下させ、内圧上昇に対する抵抗性を失わせます【文献4】。毛包壁構成成分の脆弱性の理解は、破綻メカニズムの構造生物学的基盤を提供します【文献4】。
毛包内圧上昇が毛包壁に及ぼす機械的負荷
毛包内圧の上昇は、以下の機序で毛包壁に機械的負荷を加え、破綻を促進します。内圧上昇は、生化学的破壊と相乗的に作用します。
- 皮脂と角質の蓄積:閉鎖面皰では、皮脂分泌と角質剥離が継続する一方で、排出経路が閉塞されています。この結果、毛包内容物の容積が増加し、内圧が上昇します【文献3】。
- 炎症性滲出液の貯留:炎症反応により血管透過性が亢進し、血漿成分が毛包内に漏出します。この滲出液の蓄積が、内圧をさらに上昇させます【文献3】。
- 好中球と細胞残骸の集積:大量の好中球が毛包内に集積し、死滅した細胞の残骸が蓄積します。これらの固形成分が毛包内の容積を増加させ、内圧上昇に寄与します【文献2】。
- 浸透圧効果:膿中の高濃度タンパク質とDNAは、高い浸透圧を生成し、周囲組織から水分を引き込みます。この浸透圧駆動の水分流入が、毛包内圧を持続的に上昇させます【文献2】。
毛包内圧の上昇は、物理法則に従って毛包壁に応力を発生させます【文献3】。ラプラスの法則によれば、球状構造の壁にかかる張力は、内圧と半径の積に比例します【文献3】。黄ニキビでは、毛包が球状に拡張し、内圧が上昇するため、壁にかかる張力は著しく増大します【文献3】。既に炎症によって脆弱化した毛包壁は、この機械的負荷に耐えられず、最終的に破綻します【文献3】【文献4】。破綻は、壁の最も薄い部位、または最も炎症が激しい部位で優先的に生じます【文献4】。毛包内圧上昇の機械的効果の理解は、毛包壁破綻の物理的メカニズムを説明します【文献3】【文献4】。
真皮層への炎症拡大と組織応答
毛包壁が破裂し、内容物が真皮層へ流出すると、炎症反応は急速に拡大します【文献3】。真皮層に常在する免疫細胞は、流出した異物に対して即座に応答します【文献3】。真皮マクロファージは、アクネ菌の細胞壁成分をToll様受容体2で認識し、活性化されます【文献2】。活性化されたマクロファージは、炎症性サイトカインを産生するとともに、流出した細菌と細胞残骸の貪食を試みます【文献3】。しかし、流出物の量が膨大であるため、マクロファージの処理能力は容易に飽和します【文献3】。処理しきれない異物は、真皮内に残存し、持続的な炎症刺激源となります【文献3】。特に、角質と皮脂は、マクロファージによる分解が困難であり、異物肉芽腫を形成します【文献9】。
肥満細胞の脱顆粒も、真皮層での炎症拡大に重要な役割を果たします【文献3】。肥満細胞は、アクネ菌由来のペプチドグリカンや、好中球から放出されたカチオン性タンパク質によって活性化されます【文献3】。活性化された肥満細胞は、顆粒内に貯蔵していたヒスタミン、トリプターゼ、キマーゼを急速に放出します【文献3】。ヒスタミンは、細静脈の内皮細胞に作用し、細胞間接合部を弛緩させます【文献3】。この結果、血管透過性が急激に亢進し、血漿タンパク質と水分が組織内に漏出します【文献3】。この血漿漏出が、破裂部位周囲の著明な浮腫を形成します【文献3】。トリプターゼとキマーゼは、セリンプロテアーゼであり、補体成分とキニノーゲンを活性化します【文献3】。活性化された補体とブラジキニンは、さらなる炎症反応を誘導し、炎症の自己増幅サイクルを形成します【文献3】。
線維芽細胞も、真皮層での炎症応答に関与します【文献9】。炎症性サイトカインに曝露された線維芽細胞は、活性化され、インターロイキン-6とインターロイキン-8を産生します【文献9】。また、線維芽細胞は、マトリックスメタロプロテアーゼ-1、-3、-9を産生し、真皮の膠原線維を分解します【文献9】。この膠原線維分解は、炎症細胞の組織内移動を容易にする一方で、真皮の構造的完全性を損ないます【文献9】。炎症が治癒段階に入ると、線維芽細胞は筋線維芽細胞へと分化し、創傷収縮とコラーゲン産生を開始します【文献9】。しかし、激しい炎症によって広範に破壊された真皮では、線維芽細胞の修復機能が十分に機能せず、異常な瘢痕形成が生じます【文献9】。萎縮性瘢痕は、膠原線維の量的・質的異常によって生じ、肥厚性瘢痕は、過剰なコラーゲン産生によって生じます【文献9】。このように、真皮層への炎症拡大は、急性期の組織破壊だけでなく、長期的な瘢痕形成の基盤を形成します【文献9】。
真皮マクロファージによる異物処理と肉芽腫形成
毛包から真皮へ流出した内容物に対して、マクロファージは以下の応答を示します。この応答パターンが、炎症の持続と組織リモデリングを決定します。
- 貪食作用の開始:真皮マクロファージは、流出したアクネ菌と細胞残骸を認識し、貪食を試みます。小さな粒子は効率的に貪食されますが、大きな角質塊と皮脂の塊は貪食が困難です【文献3】。
- M1型への極性化:異物認識により、マクロファージはM1型の炎症促進性表現型へと極性化します。M1型マクロファージは、腫瘍壊死因子-α、インターロイキン-1β、インターロイキン-12を産生し、炎症反応を増幅します【文献3】。
- 多核巨細胞への融合:貪食不能な大型異物に対して、複数のマクロファージが融合し、多核巨細胞を形成します。多核巨細胞は、異物を取り囲み、隔離しようとしますが、角質と皮脂の完全な分解は達成できません【文献9】。
- 肉芽腫の形成:貪食不能な異物の周囲には、マクロファージ、多核巨細胞、リンパ球、そして線維芽細胞が層状に配列し、異物肉芽腫を形成します。この構造は、慢性炎症の組織学的特徴です【文献9】。
異物肉芽腫の形成は、黄ニキビにおける炎症の慢性化を示します【文献9】。肉芽腫内では、マクロファージが持続的に炎症性サイトカインを産生し、周囲組織への炎症波及が継続します【文献9】。また、肉芽腫の辺縁では、線維芽細胞がコラーゲンを産生し、異物を線維性組織で被包しようとします【文献9】。この線維化プロセスが、最終的には瘢痕組織を形成します【文献9】。マクロファージによる異物処理機構の理解は、黄ニキビにおける慢性炎症と瘢痕形成の関連を説明します【文献9】。
血管透過性亢進と炎症性浮腫の形成
真皮層への炎症拡大時には、以下の機序で血管透過性が亢進し、著明な浮腫が形成されます。浮腫は、炎症の空間的拡大を促進します。
- ヒスタミンによる即時型反応:肥満細胞から放出されたヒスタミンは、細静脈の内皮細胞上のH1受容体に結合し、細胞内カルシウム濃度を上昇させます。この変化により、内皮細胞は収縮し、細胞間接合部が開大します【文献3】。
- 血管内皮増殖因子の作用:炎症性サイトカインは、血管内皮細胞と線維芽細胞に血管内皮増殖因子の産生を誘導します。血管内皮増殖因子は、内皮細胞の透過性を持続的に亢進させます【文献3】。
- ブラジキニンの生成:肥満細胞のキマーゼがキニノーゲンを切断し、ブラジキニンを生成します。ブラジキニンは、強力な血管拡張作用と透過性亢進作用を持ちます【文献3】。
- ロイコトリエンの作用:好中球とマクロファージが産生するロイコトリエンB4とC4は、血管透過性を亢進させるとともに、好中球の遊走を促進します【文献3】。
これらの機序により、破裂部位の周囲には著明な血管透過性亢進が生じます【文献3】。血管から漏出した血漿タンパク質と水分は、組織間質に貯留し、浮腫を形成します【文献3】。浮腫は、組織の腫脹と圧痛を引き起こすとともに、炎症性メディエーターの拡散を促進します【文献3】。また、浮腫による組織内圧の上昇は、毛細血管を圧迫し、局所血流を低下させます【文献3】。この血流低下は、組織の低酸素状態を引き起こし、組織障害をさらに増悪させます【文献3】。血管透過性亢進と浮腫形成の理解は、黄ニキビにおける炎症の空間的拡大を説明します【文献3】。
膠原線維とエラスチン線維の分解機構
真皮の構造的完全性は、膠原線維とエラスチン線維によって維持されています【文献9】。これらの線維は、皮膚の引張強度と弾性を提供し、組織の形態を保持します【文献9】。しかし、黄ニキビの病変部では、これらの線維が広範に分解されます【文献9】。線維分解の主要な担い手は、マトリックスメタロプロテアーゼです【文献9】。マトリックスメタロプロテアーゼは、亜鉛依存性のエンドペプチダーゼであり、細胞外マトリックスタンパク質を特異的に分解します【文献9】。黄ニキビの病変部では、マトリックスメタロプロテアーゼ-1、-2、-3、-8、-9が高レベルで発現しています【文献9】。これらの酵素は、ケラチノサイト、線維芽細胞、マクロファージ、そして好中球から産生されます【文献9】。
マトリックスメタロプロテアーゼ-1は、コラゲナーゼとも呼ばれ、I型とIII型膠原のネイティブな三重らせん構造を切断する能力を持ちます【文献9】。この酵素は、膠原分子内の特定のGly-Ile結合を認識し、分子を3/4と1/4の断片に切断します【文献9】。切断された膠原断片は、体温で自然に変性し、ゼラチンとなります【文献9】。ゼラチンは、マトリックスメタロプロテアーゼ-2と-9によってさらに分解されます【文献9】。マトリックスメタロプロテアーゼ-3は、ストロメライシン-1とも呼ばれ、広範な基質特異性を持ちます【文献9】。この酵素は、プロテオグリカン、フィブロネクチン、ラミニン、そしてエラスチンを分解します【文献9】。また、マトリックスメタロプロテアーゼ-3は、他のマトリックスメタロプロテアーゼの前駆体を活性化する機能も持ちます【文献9】。マトリックスメタロプロテアーゼ-8と-9は、好中球から大量に放出され、膠原線維の急速な分解を引き起こします【文献2】【文献9】。
エラスチン線維の分解は、主に好中球エラスターゼによって媒介されます【文献2】。好中球エラスターゼは、セリンプロテアーゼであり、エラスチンを効率的に分解する特性を持ちます【文献2】。エラスチンは、高度に架橋された疎水性タンパク質であり、通常のプロテアーゼでは分解が困難です【文献2】。しかし、好中球エラスターゼは、エラスチンのアラニンとバリンに富む疎水性領域を特異的に認識し、切断します【文献2】。黄ニキビの病変部では、好中球エラスターゼの活性が著しく上昇しており、エラスチン線維の広範な分解が生じています【文献2】。エラスチン線維の喪失は、真皮の弾性回復力を低下させ、組織の機械的特性を変化させます【文献9】。膠原線維とエラスチン線維の分解は、可逆的な変化ではなく、炎症が治癒した後も、線維の量的・質的異常が残存します【文献9】。この不可逆的な線維破壊が、萎縮性瘢痕の形成基盤となります【文献9】。
マトリックスメタロプロテアーゼの発現調節機構
黄ニキビの病変部におけるマトリックスメタロプロテアーゼの発現は、以下の機序で調節されます。これらの調節機構の理解は、線維分解の分子基盤を説明します。
- 炎症性サイトカインによる転写誘導:インターロイキン-1βと腫瘍壊死因子-αは、線維芽細胞とケラチノサイトに作用し、AP-1転写因子を活性化します。AP-1は、マトリックスメタロプロテアーゼ遺伝子のプロモーター領域に結合し、転写を促進します【文献9】。
- 活性酸素種による発現増強:活性酸素種は、細胞内シグナル伝達経路を活性化し、マトリックスメタロプロテアーゼの発現を増強します。特に、MAPKとNF-κB経路の活性化が重要です【文献2】【文献9】。
- プロ酵素の活性化:マトリックスメタロプロテアーゼは、不活性なプロ酵素として分泌され、細胞外で活性化されます。活性化は、プラスミンやマトリックスメタロプロテアーゼ-3によって触媒されます【文献9】。
- 組織メタロプロテアーゼ阻害因子の減少:正常組織では、組織メタロプロテアーゼ阻害因子がマトリックスメタロプロテアーゼの活性を制御しています。しかし、炎症部位では、この阻害因子の相対的濃度が低下し、プロテアーゼ活性が優位となります【文献9】。
これらの調節機構により、黄ニキビの病変部では、マトリックスメタロプロテアーゼの発現と活性が著しく上昇します【文献9】。特に、炎症性サイトカインと活性酸素種の相乗効果は、プロテアーゼ発現を最大化します【文献2】【文献9】。また、組織メタロプロテアーゼ阻害因子の相対的減少は、分解と合成のバランスを分解側に傾け、組織破壊を促進します【文献9】。マトリックスメタロプロテアーゼの発現調節機構の理解は、真皮線維分解の分子機序を説明します【文献9】。
線維分解産物の生物学的活性
膠原線維とエラスチン線維の分解によって生成される断片は、以下の生物学的活性を持ちます。これらの活性が、炎症反応をさらに増幅します。
- 走化性活性:膠原断片とエラスチン断片は、好中球とマクロファージに対する走化性因子として機能します。これらの断片は、炎症細胞を分解部位へと誘導し、炎症の拡大を促進します【文献9】。
- 血管新生促進活性:特定のサイズの膠原断片は、血管内皮細胞の増殖と遊走を促進し、血管新生を誘導します。血管新生は、炎症組織への栄養供給を増加させますが、同時に炎症細胞の供給も増加させます【文献9】。
- 線維芽細胞活性化:線維分解産物は、線維芽細胞を刺激し、さらなるマトリックスメタロプロテアーゼの産生を誘導します。この正のフィードバックが、組織破壊を加速させます【文献9】。
- インテグリン結合:一部の膠原断片は、細胞表面のインテグリンに結合し、細胞内シグナル伝達を活性化します。このシグナルは、細胞の遊走、増殖、そして炎症性メディエーター産生に影響を与えます【文献9】。
これらの生物学的活性により、線維分解は単なる組織破壊ではなく、炎症反応を能動的に調節するプロセスとして機能します【文献9】。特に、走化性活性と線維芽細胞活性化は、炎症の自己増幅サイクルを形成します【文献9】。また、血管新生促進活性は、炎症組織のリモデリングと肉芽組織形成を開始させます【文献9】。このように線維分解産物の生物学的活性の理解することで、黄ニキビにおける組織破壊と修復の複雑な相互作用を説明できます【文献9】。
まとめ
黄ニキビは、膿疱性痤瘡として定義され、尋常性痤瘡の最も重症化した臨床像を示します【文献1】。組織学的には、毛包壁の著しい破壊と好中球を主体とする炎症性細胞の密集が確認され、中心部の黄白色調は炎症性滲出物の光学的特性に由来します【文献3】。この病変は、自発痛や圧痛を伴い、治癒後も萎縮性瘢痕や色素沈着を残す傾向があります【文献9】。黄ニキビの本質は、単なる表層的な炎症ではなく、皮膚の深部構造に及ぶ破壊的プロセスとして理解されます【文献4】。
ニキビの進行は、微小面皰から白ニキビ、赤ニキビを経て、黄ニキビへと段階的に移行します【文献3】【文献4】。微小面皰では、毛包漏斗部における角化異常と皮脂蓄積が生じ、酸素分圧の低下によりアクネ菌の増殖に有利な嫌気性環境が形成されます【文献3】【文献4】。白ニキビでは、毛包開口部の完全閉塞により、アクネ菌数が急速に増加します【文献3】。赤ニキビへの移行では、アクネ菌のリパーゼが皮脂を分解して生成した遊離脂肪酸が毛包上皮を刺激し、インターロイキン-1αの産生を誘導します【文献3】【文献5】。この段階で、Toll様受容体2を介したシグナル伝達が活性化され、炎症性サイトカインの産生が開始されます【文献2】。黄ニキビへの進行では、好中球の大量浸潤と毛包壁の破綻が生じ、膿疱性病変が確立します【文献4】。
黄ニキビ形成の分子生物学的基盤は、NLRP3インフラマソームの活性化にあります【文献6】。アクネ菌感染細胞では、細胞内カリウムイオン濃度の低下と活性酸素種の産生がNLRP3を活性化し、カスパーゼ-1を介してプロインターロイキン-1βが成熟型サイトカインへと変換されます【文献2】【文献6】。脂腺細胞におけるインフラマソーム活性化も重要であり、脂腺細胞は脂質産生と免疫応答の両機能を担います【文献7】。成熟インターロイキン-1βは、インターロイキン-8の産生を誘導し、好中球の持続的な動員を維持します【文献2】。炎症性サイトカインネットワークでは、インターロイキン-1β、インターロイキン-8、腫瘍壊死因子-αが相乗的に作用し、炎症反応を増幅します【文献2】。好中球が産生する活性酸素種は、組織の直接的な酸化障害を引き起こすとともに、マトリックスメタロプロテアーゼの発現を誘導し、間接的にも組織破壊を促進します【文献2】【文献10】。
毛包内環境の変化は、アクネ菌の病原性発現を促進します【文献3】。閉鎖面皰内では、酸素分圧が低下し、pHが酸性化し、浸透圧が上昇します【文献3】。これらの物理化学的変化は、アクネ菌の選択的増殖を促進するとともに、毛包上皮のバリア機能を低下させます【文献3】。アクネ菌が産生するリパーゼは、皮脂を分解して遊離脂肪酸を生成し、ケラチノサイトを刺激します【文献3】。プロテアーゼは、毛包壁の細胞間接着タンパク質と基底膜を分解し、組織の構造的完全性を損ないます【文献3】。細胞壁成分であるペプチドグリカンとリポテイコ酸は、Toll様受容体2を刺激し、炎症性サイトカインの産生を誘導します【文献2】。バイオフィルム形成は、アクネ菌を宿主の免疫攻撃から保護し、炎症の慢性化を促進します【文献3】。
好中球の動員と活性化は、膿形成の中心的メカニズムです【文献2】。インターロイキン-8は、血管内皮細胞を活性化し、接着分子の発現を誘導します【文献2】。好中球は、セレクチン-リガンド相互作用によるローリング、インテグリン-ICAM相互作用による強固な接着、そしてPECAM-1を介した血管外遊出という段階的プロセスを経て、炎症部位へと集積します【文献2】。組織内に遊走した好中球は、インターロイキン-8、補体C5a、GM-CSFといった複数のシグナル分子によって活性化されます【文献2】。活性化された好中球は、NADPHオキシダーゼにより活性酸素種を産生し、リソソーム顆粒からエラスターゼ、カテプシンG、ミエロペルオキシダーゼを放出します【文献2】。これらの殺菌因子は、細菌だけでなく周囲の宿主組織にも障害を与えます【文献2】。好中球の多くは、激しい炎症環境下で壊死に至り、その残骸が膿の主要成分を構成します【文献2】。
毛包壁の破裂は、酵素的分解、酸化障害、そして機械的負荷の複合作用によって生じます【文献4】。好中球エラスターゼとマトリックスメタロプロテアーゼは、基底膜のIV型膠原とラミニン、そして結合組織鞘の膠原線維を段階的に分解します【文献2】【文献4】。活性酸素種は、膠原線維の架橋結合を切断し、組織の機械的強度を低下させます【文献2】。同時に、皮脂・角質の蓄積、炎症性滲出液の貯留、好中球の集積により、毛包内圧が上昇し、脆弱化した毛包壁に持続的な機械的負荷を加えます【文献3】。毛包壁が破裂すると、内容物が真皮層へと流出し、真皮マクロファージの活性化、肥満細胞の脱顆粒、血管透過性の亢進が生じます【文献3】。流出した角質と皮脂は、異物肉芽腫を形成し、慢性炎症の持続を招きます【文献9】。真皮層では、マトリックスメタロプロテアーゼと好中球エラスターゼによる膠原線維とエラスチン線維の分解が広範に生じ、この不可逆的な線維破壊が、萎縮性瘢痕の形成基盤となります【文献9】。
黄ニキビの形成は、毛包内環境の変化、アクネ菌の病原性発現、宿主免疫応答の過剰な活性化、そして組織破壊機構の作動が、段階的に統合された結果として生じます【文献1】【文献2】【文献3】【文献4】。各段階では、特異的な分子機構と細胞応答が作動し、炎症反応は自己増幅する性質を持ちます【文献2】。好中球が放出する活性酸素種とプロテアーゼは、殺菌機構として機能する一方で、宿主組織にも無差別な障害を与えるという副次的効果を持ちます【文献2】。この非特異的な組織障害が、黄ニキビにおける広範な毛包壁破壊と真皮障害の主要な機序となります【文献2】【文献4】。黄ニキビは、複雑な多因子性病態であり、分子レベル、細胞レベル、組織レベルの各階層における詳細な知見を統合的に理解することによって、その本質的なメカニズムを説明できます【文献1】【文献2】【文献3】【文献4】【文献9】。
専門用語一覧
- 異物肉芽腫:貪食不能な異物の周囲に、マクロファージ、多核巨細胞、リンパ球、線維芽細胞が層状に配列して形成される慢性炎症の組織学的構造です。
- インターロイキン-1α(IL-1α):ケラチノサイトから放出される初期炎症メディエーターであり、炎症反応の開始シグナルとして機能します。
- インターロイキン-1β(IL-1β):炎症性サイトカインの中核であり、インフラマソームによって活性化され、他の炎症性メディエーターの産生を誘導します。
- インターロイキン-6(IL-6):炎症反応の慢性化に寄与するサイトカインであり、T細胞の分化と急性期タンパク質産生を促進します。
- インターロイキン-8(IL-8):最も強力な好中球走化因子であり、好中球の動員と活性化を誘導します。
- インターロイキン-17(IL-17):Th17細胞が産生するサイトカインであり、好中球の動員を増強し、炎症反応を慢性化させます。
- インテグリン:細胞表面に発現する接着分子であり、リガンドへの結合により細胞の接着と遊走を制御します。好中球の血管外遊出に必須です。
- インフラマソーム:細胞質内で形成される多タンパク質複合体であり、炎症性サイトカインの成熟と放出を制御します。
- カテプシンG:好中球のリソソーム顆粒に含まれるシステインプロテアーゼであり、細菌と宿主組織のタンパク質を分解します。
- ケモカイン:走化性因子として機能するサイトカインの総称であり、炎症細胞の組織内遊走を誘導します。
- 好中球エラスターゼ:好中球が産生するセリンプロテアーゼであり、エラスチン線維と膠原線維を効率的に分解します。
- セレクチン:血管内皮細胞上に発現する接着分子であり、好中球のローリングを媒介します。P-セレクチンとE-セレクチンが存在します。
- DAMPs(damage-associated molecular patterns):組織障害時に細胞から放出される内因性分子であり、免疫系を活性化して炎症反応を誘導します。
- Th17細胞:インターロイキン-17を産生するヘルパーT細胞のサブセットであり、好中球の動員と炎症の慢性化を促進します。
- Toll様受容体2(TLR2):パターン認識受容体の一種であり、アクネ菌の細胞壁成分を認識してNF-κB経路を活性化します。
- バイオフィルム:細菌が産生する細胞外マトリックスに包埋された細菌集団であり、宿主の免疫攻撃から保護されます。
- 白血球接着カスケード:好中球が血管内から組織内へ遊走する多段階プロセスであり、ローリング、活性化、強固な接着、血管外遊出から構成されます。
- ファゴソーム:好中球が細菌を貪食した際に形成される細胞内小胞であり、リソソームと融合して殺菌環境を形成します。
- 補体系:血清中のタンパク質群が連鎖的に活性化される免疫系であり、C5aなどの走化性因子を生成して好中球を動員します。
- マトリックスメタロプロテアーゼ(MMP):亜鉛依存性のエンドペプチダーゼであり、細胞外マトリックスタンパク質を特異的に分解します。
- ミエロペルオキシダーゼ(MPO):好中球の顆粒に含まれる酵素であり、過酸化水素と塩化物イオンから次亜塩素酸を生成します。
- MyD88:Toll様受容体のシグナル伝達に関与するアダプタータンパク質であり、NF-κB経路を活性化します。
- NADPHオキシダーゼ:好中球の細胞膜に存在する酵素複合体であり、分子状酸素からスーパーオキシドアニオンを生成します。
- NETs(neutrophil extracellular traps):好中球が放出するDNAとヒストンからなる網状構造であり、細菌を捕捉しますが組織障害も引き起こします。
- NF-κB(nuclear factor kappa B):転写因子であり、炎症性サイトカイン遺伝子の発現を制御します。
- NLRP3インフラマソーム:NLRP3タンパク質、ASC、プロカスパーゼ-1から構成される多タンパク質複合体であり、インターロイキン-1βの成熟を制御します。
- PECAM-1(platelet endothelial cell adhesion molecule-1):好中球と内皮細胞の両方に発現する接着分子であり、好中球の内皮細胞間接合部通過を促進します。
- ICAM-1(intercellular adhesion molecule-1):血管内皮細胞上に発現する接着分子であり、好中球のインテグリンと結合して強固な接着を媒介します。
- リソソーム:細胞内小器官であり、好中球では抗菌ペプチドとプロテアーゼを貯蔵する顆粒として機能します。
- ロイコトリエンB4:アラキドン酸代謝経路から生成される脂質メディエーターであり、好中球の走化性と活性化を促進します。
参考文献一覧
- Bhate K, Williams HC. Epidemiology of acne vulgaris. Br J Dermatol. 2013;168(3):474-485.
- Kistowska M, Gehrke S, Jankovic D, et al. IL-1β drives inflammatory responses to Propionibacterium acnes in vitro and in vivo. J Invest Dermatol. 2014;134(3):677-685.
- Jeremy AH, Holland DB, Roberts SG, Thomson KF, Cunliffe WJ. Inflammatory events are involved in acne lesion initiation. J Invest Dermatol. 2003;121(1):20-27.
- Do TT, Zarkhin S, Orringer JS, et al. Computer-assisted alignment and tracking of acne lesions indicate that most inflammatory lesions arise from comedones and de novo. J Am Acad Dermatol. 2008;58(4):603-608.
- Ingham E, Eady EA, Goodwin CE, Cove JH, Cunliffe WJ. Pro-inflammatory levels of interleukin-1 alpha-like bioactivity are present in the majority of open comedones in acne vulgaris. J Invest Dermatol. 1992;98(6):895-901.
- Qin M, Pirouz A, Kim MH, Krutzik SR, Garbán HJ, Kim J. Propionibacterium acnes induces IL-1β secretion via the NLRP3 inflammasome in human monocytes. J Invest Dermatol. 2014;134(2):381-388.
- Li ZJ, Choi DK, Sohn KC, et al. Propionibacterium acnes activates the NLRP3 inflammasome in human sebocytes. J Invest Dermatol. 2014;134(11):2747-2756.
- Tanghetti EA. The role of inflammation in the pathology of acne. J Clin Aesthet Dermatol. 2013;6(9):27-35.
- Holland DB, Jeremy AH, Roberts SG, et al. Inflammation in acne scarring: a comparison of the responses in lesions from patients prone and not prone to scar. Br J Dermatol. 2004;150(1):72-81.
- Zouboulis CC, Jourdan E, Picardo M. Acne is an inflammatory disease and alterations of sebum composition initiate acne lesions. J Eur Acad Dermatol Venereol. 2014;28(5):527-532.
執筆者
中濵数理2-300x294.png)
■博士(工学)中濵数理
- 由風BIOメディカル株式会社 代表取締役社長
- 沖縄再生医療センター:センター長
- 一般社団法人日本スキンケア協会:顧問
- 日本再生医療学会:正会員
- 特定非営利活動法人日本免疫学会:正会員
- 日本バイオマテリアル学会:正会員
- 公益社団法人高分子学会:正会員
- X認証アカウント:@kazu197508




